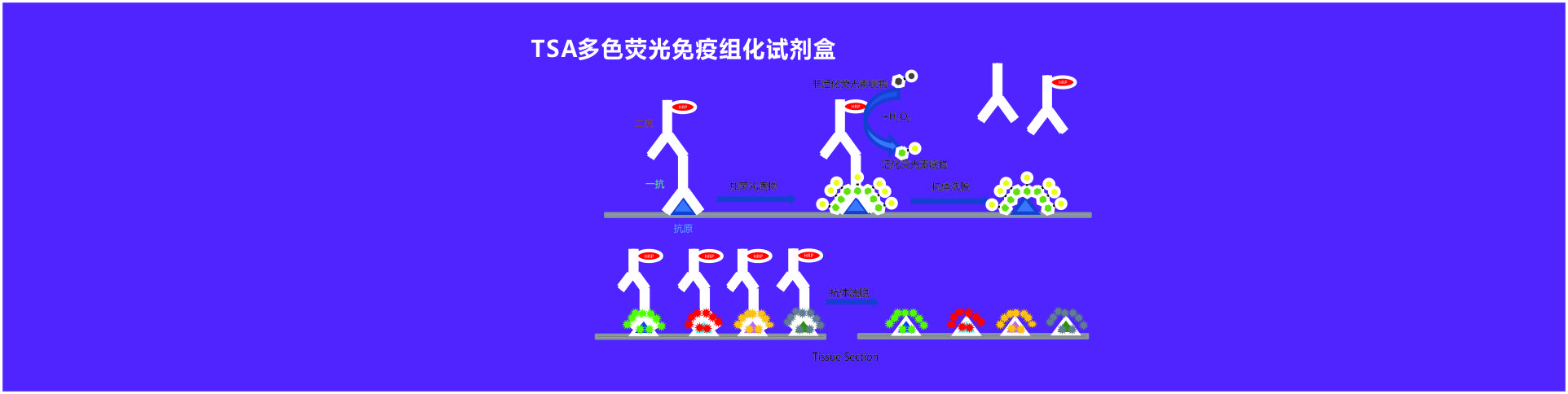
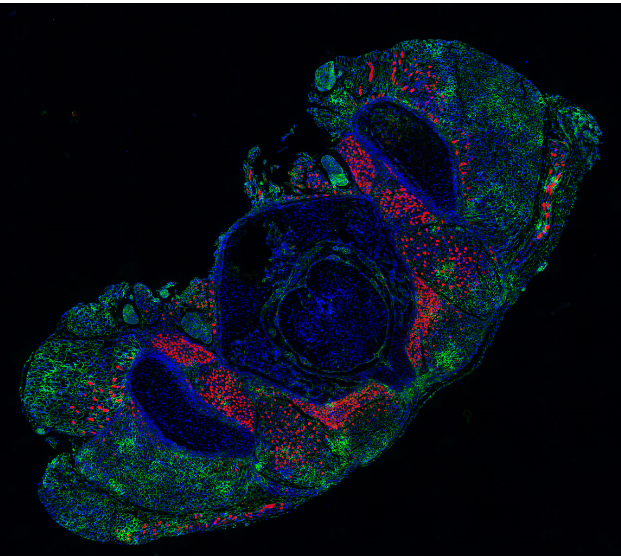
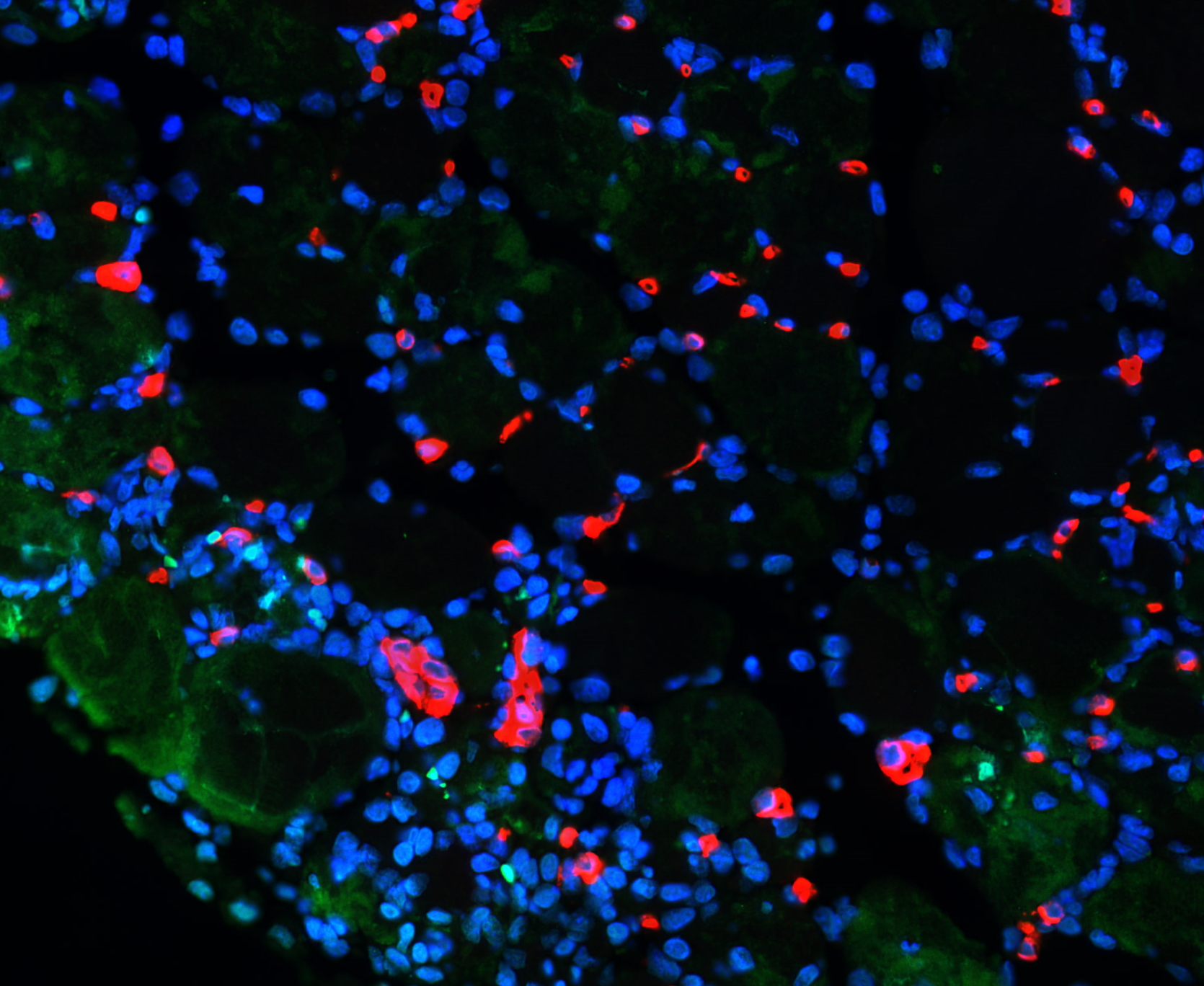
精选单品
查看更多热门解决方案
查看更多-
ChIP实验指南
ChIP概述
ChIP(Chromatin Immunoprecipitation)技术的主要目的是研究目的蛋白(包括:修饰组 蛋白,转录因子,辅因子及其他染色质蛋白)在染色质上的定位及丰度分析。
1993年James Broach在Genes&Dev上首次描述了染色质免疫共沉淀(ChIP)技术,研究酵 母中组蛋白乙酰化状态下的转录基因沉默。而此项技术第一次在哺乳动物细胞中成功还要归 功于Richard Treisman课题组,他们将成果发表在了1998年的Cell上。
从此ChIP走过了一段漫长的发展之路,经过全球范围内无数个实验室,不同物种样本的 尝试,才使得ChIP技术成为研究蛋白-DNA互作的经典实验方法。其下游分析也从终点PCR (endpoint-PCR)发展到如今的高通量测序(NGS,Next Generation Sequence)。
ChIP实验的基础步骤是使用甲醛溶液将DNA和作用蛋白交联固定在一起后,提取染色质 并将染色质剪切到一定的片段大小,再用染色质蛋白特异性抗体,通过免疫沉淀富集感兴趣 的染色质片段。
最初检测感兴趣的DNA是通过固定在硝化纤维素上并用与目标位点互补的DNA探针分析ChIP结果,这种方法限制了ChIP技术的灵敏度,因此基于PCR的分析检测方法应运而生,其 中包括终点PCR检测,荧光定量PCR检测。
ChIP在表观遗传学中的应用
ChIP是研究表观遗传标记映射至基因组个别位点的主要技术,表观遗传学研究主要包括组蛋白与基因表达间的关系,或是研究非组蛋白蛋白与染色质作用如何影响了基因表达,如转录因子。
ChIP技术可以帮我们解答特异性修饰组蛋白或转录因子在染色质上是如何分布的,通过分析它们的染色质定位可以为解码目的蛋白的功能提供帮助。以组蛋白修饰为例,组蛋白H3的第四位赖氨酸三甲基化(H3K4me3)主要定位在转录活跃基因的启动子CpG岛上,这提示我们H3K4me3跟转录激活相关,而组蛋白H3K27me3主要分布在转录抑制的基因上,说明H3K27me3跟转录抑制相关。
另一方面,在转录调控研究中,如果我们知道某种转录因子定位在哪些基因的启动子上,便可知这个转录因子调控哪些基因表达,其丰度的多少可以揭示这种转录因子对不同基因的调控强度。
这都需要利用免疫共沉淀技术特异富集染色质位点。ChIP技术在实验层面上是非常具有挑战性的,许多因素都可能导致其失败,因此,最好使用经过良好验证的抗体和可靠的试剂来进行这些分析。
Active Motif 研发出了ChIP-IT®系列产品,针对不同实验因素,优化试剂和实验方法,使得ChIP实验灵敏度得到大幅提高。
O 提供实验全套解决方案,使实验轻松简单
O 选用protein G 包被的磁珠,使1天完成ChIP实验成为可能
O 低细胞,转录因子不再是ChIP实验道路上的阻碍
O 260多种ChIP级抗体
ChIP实验关键步骤
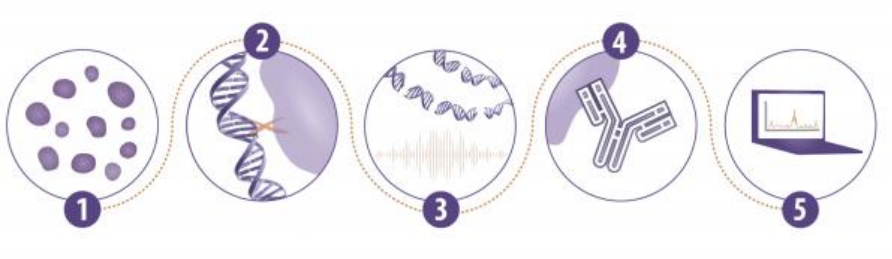
ChIP实验过程步骤繁琐,想要得到好的ChIP结果,每一步都需要细心仔细。
其中,ChIP实验中有五个关键步骤尤为重要。
1. 起始样本:每一个ChIP实验的开展,都离不开样本的选择,ChIP实验可使用细胞或组 织样本。不同的样本对应的起始量也不同。
2. 交联固定:通常进行ChIP实验时,细胞需要经过固定,保证蛋白与DNA的交联。大多 数的实验方法都是采用甲醛进行细胞固定,但也有使用不同的固定条件和固定剂。
3. 染色质片段化:制备片段化的染色质通常使用超声法,在一些条件下也会使用酶切
法。
4. 免疫沉淀:制备染色质后,下一步是实际的免疫沉淀(IP)步骤。使用的抗体是至关 重要的,决定是否使用磁性或琼脂糖珠也是至关重要的。
5. 下游数据分析:ChIP实验最后一步是数据的分析,通常是qPCR或者高通量测序。
ChIP实验样本的准备
ChIP实验可以使用多样的样本类型,如组织,细胞系,FFPE等。但传统ChIP实验的开展 往往需要上百万的细胞或者大量的组织才能够满足需求,使得样本量成为了获得优良ChIP结 果的一大阻碍。
特别是对于某些样本类型,如原代细胞和干细胞,有时很难获得足够的细胞。再如一些 特殊样本,如PBMC,或者石蜡样本,用传统的ChIP方法很难得到优良的数据结果。
这就需要针对不同的样本类型优化ChIP实验。最近,随着专为低细胞起始量ChIP试剂盒 的开发,ChIP所需的细胞数量已经下降了很多。这些试剂盒已经开始允许研究人员使用几千 而不是数百万的细胞进行实验,而且每天都有新技术问世,使细胞起始需求量进一步下降, 如CUT&Tag技术(可在本书封底扫码公众号,下载/申领《CUT&Tag完全指南》)。
Active Motif基于不同ChIP实验的需求,研发出具有针对性的试剂盒产品。
ChIP试剂盒选择指南
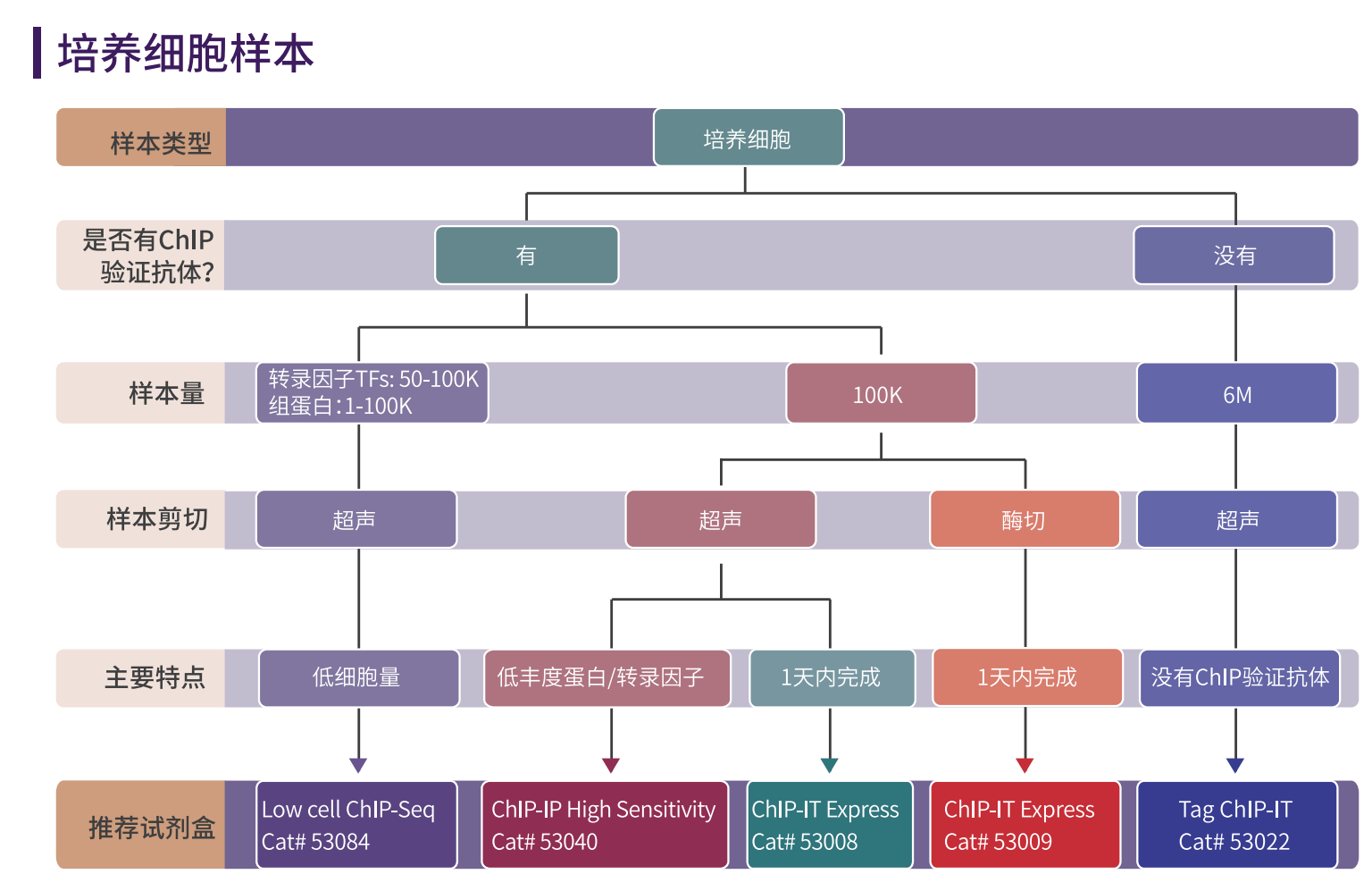
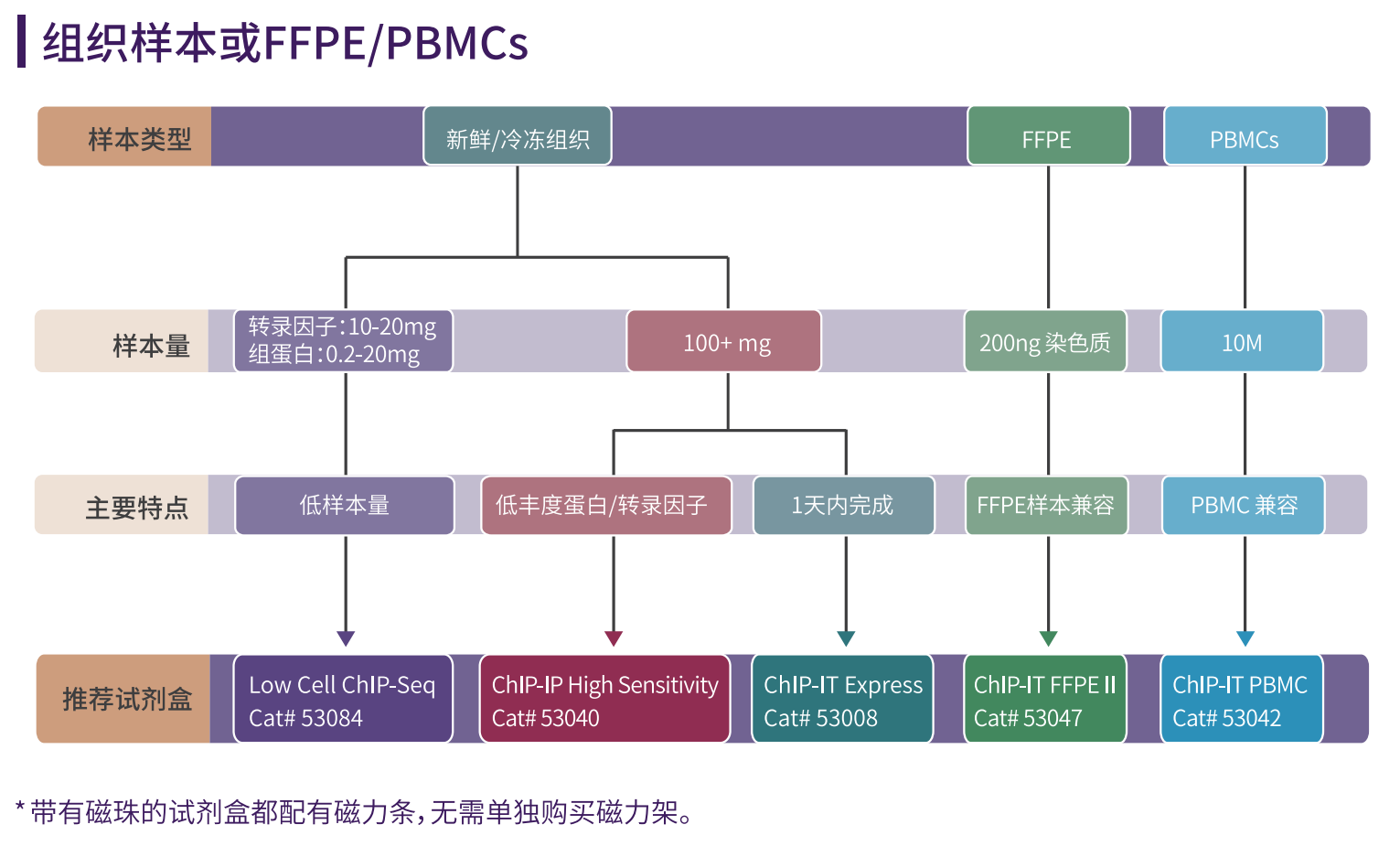
如何正确固定实验样本
ChIP实验可以使用许多不同的样品类型,所以ChIP实验的一个重要环节就如何处理样本,在大多数ChIP实验中,都需要固定环节,固定是为了将DNA与相关蛋白质交联,不同的细胞和组织类型需要不同的固定方案。需要考虑使用的何种类型的固定剂和固定时长。
ChIP技术用到的最主要的信息保存方式是甲醛交联,最早的ChIP技术并不是使用甲醛交联的,只是后来发现甲醛能更好的保存蛋白与DNA的信息,所以后来除了用于检测组蛋白修饰分布的Native ChIP以外,其他的ChIP基本上都需要用甲醛交联。

在实际使用甲醛进行交联实验的时候,甲醛浓度和交联时间都是有严格要求的。
1.一般的甲醛交联都选用1%的甲醛浓度,室温固定10-15分钟。时间太短的话,交联反应 进行的不彻底,很多蛋白与DNA的结合不是很牢固,交联时间太长的话,会导致后续超声非 常困难,而增加超声时间或功率会破坏目的蛋白本身的结构,进而导致ChIP结果不理想。
2. 为了尽可能保存细胞原始状态下的目的蛋白在染色质上的定位,甲醛交联之前,细胞 需要尽可能少的被人为处理。可直接将甲醛加入培养基或将细胞培养基换成含有1%甲醛的PBS 交联,这样会比胰酶消化细胞以后再交联效果更好。
3. 甲醛交联反应结束之后,需要马上加入相对甲醛过量的甘氨酸(一般甘氨酸终浓度为125mM)与甲醛反应,终止交联反应。终止交联之后,样本需要经过PBS清洗(如果细胞数 量比较少的话,可以在PBS里加入0.1%-0.5% NP-40,这样细胞在转移时不会粘在管壁或培养皿 上)。
4. 组织的交联相比细胞交联要复杂一些。虽然甲醛可以很容易的透过细胞,但是大的组 织块还是不太容易交联的很均一,大的组织块交联之前需要切成小块。但组织块并不是越小 越好,组织块切的越小,细胞破坏的越严重。所以一般建议将组织块切成1-3 mm3大小。组织 的交联时间一般可以延长到15 min,这样能保证组织的充分交联。
5. 考虑到甲醛并不能很好的交联距离大于2埃的DNA和蛋白,还有一些文献报道用分子 长度更长的交联剂(一般是双官能团的亚氨酸酯类)配合甲醛对蛋白和DNA进行交联。比 如,DTBP,DMA,DSG,DSP,EGS。
染色质片段化
样本固定后,必须对其进行裂解和超声处理,以产生可溶性染色质,用于免疫沉淀反 应。一般染色质片段的期望大小在200到1000个碱基对之间,而想要得到好的染色质结果还需 要考虑多个方面。
获得细胞核中固定的染色质
在固定之后,需要从细胞核中获得片段大小足够小的染色质,才能满足抗体有效结合沉 淀。
虽然分离细胞核并不是一个绝对必需的步骤,但在片段化染色质之前,通过分离细胞 核,改善ChIP结果不失为一个好的选择。Active Motif使用dounce研磨杵(cat#40401和40415) 分离细胞核,将核分离作为ChIP实验的的标准实验步骤。这是因为我们发现细胞核的分离是 生成高质量数据的重要步骤。在细胞核被分离后,能够更轻松的获得可溶性染色质。
片段化染色质—— 哪一种方法才是最佳选择?
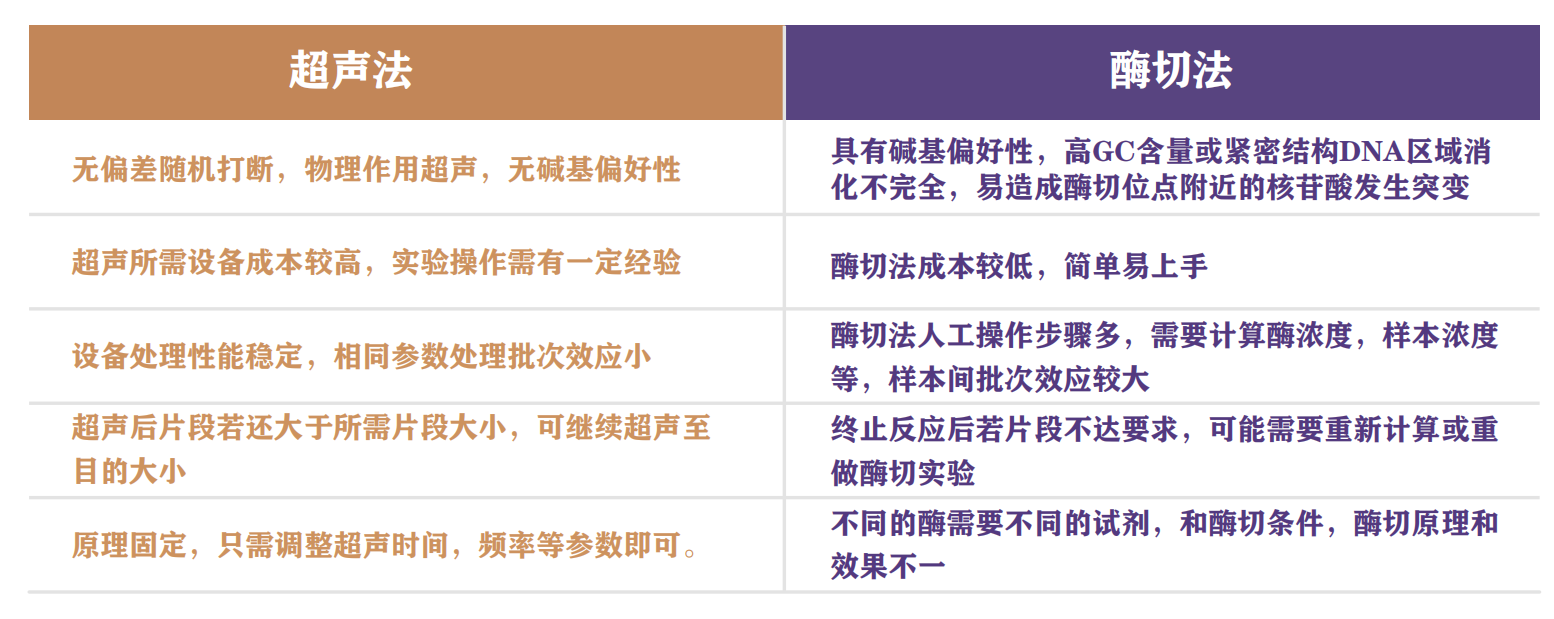
我们可以通过超声法或酶切法将染色质片段化。无论是超声或者酶切,都需要将染色质 片段化至200-1000个碱基对范围内,要确保DNA片段不能过大或者过小。超声法作为经典的方 法,被广泛的应用于ChIP实验,但针对不同的起始样本,需要对超声条件进行摸索和优化。
优化超声条件以获得最佳片段化效果
针对不同的样本类型,需要摸索对应的超声条件。但当某一细胞系,或者组织类型,确 定其超声条件后,再次使用同类型样本时,可使用相同方法进行超声。另外,像一些细胞类 型或组织由于其自身特性,也会对超声制备染色质造成困难。
样品制备本身有三个因素会对超声效果产生影响:
1. 超声用的buffer。这其中尤其以SDS的影响最大,SDS浓度越高,DNA越容易被打断。同 时盐离子和其他去垢剂浓度都会对超声产生影响,一般认为盐离子或去垢剂浓度越高,DNA 越容易被打断。
2. 细胞密度。超声时的细胞密度越高,DNA越不容易被打断。所以建议细胞密度应小于107 cells/ml裂解液。
3. 细胞类型。不同细胞类型间,超声效果差异也很大。相对于常用的肿瘤细胞系,很多原代培养的细胞以及组织细胞的染色质超声破碎会更困难些。例如,T细胞往往很难进行超声 检测,因为它们是非常小、紧密的细胞,很难打开,所以需要不同的溶解和超声条件才能实 现最好的结果。
关于超声参数选择及优化技巧参见附录二(P24)。
使用酶切法获得片段化染色质
大多数研究人员更喜欢用超声波来切割DNA,因为它高效且随机,但用超声法也有其 局限性,如需要专门的超声设备,或需要根据样本优化超声条件。一些研究者没有超声设 备,或者希望以一种温和的方式处理DNA,这种情况下酶切法不失为一个好的选择,如使用 微球菌核酸酶的剪切法(如MNase)。MNase是一种优先切割AT富集序列区域的酶,它可以 在一段时间内生成所需大小的染色质片段。而让大多数科学家对酶切法产生顾虑的主要原因 是其切割DNA具有偏好性。随着技术的发展,一些较新的染色质分析方法使用MNase与抗体 结合,使得酶切法能够应用于较低的细胞起始量(CUT&RUN技术)。
使用酶切法片段化染色质处理不同类型样本时也需要对处理条件进行优化,主要包括 酶的用量及处理时间的优化。
IP反应
抗体是决定IP结果的关键
超声之后的IP过程是ChIP成功与否的关键。首先是抗体。适用于ChIP的最佳抗体一直是 该领域的争论。多克隆比单克隆好吗?这不一定,这取决于细节。重组抗体的出现,使得争 论进入新的层面,Active Motif现在正在以重组蛋白的形式生产抗体,与传统的单克隆抗体相 比,重组蛋白抗体的一致性更高。
我们将在下面讨论每种类型的好处,以帮助您决定在实验中最好使用哪种类型。

当涉及ChIP实验时,特异性其实比抗体类型更重要
为ChIP实验选择抗体时, 最重要的是评估它是否在固定条件下以高度特异性识别靶标蛋 白质,以及它是否能够经受长时间的IP和清洗步骤保持高结合力。在ChIP问世的早期,许多 研究人员倾向于使用多克隆抗体,因多克隆抗体通常包含抗某一抗原的不同表位的抗体, 包 括一些变性的表位,所以,在固定的样本中多克隆抗体可能较单克隆抗体更具有优势。
然而现在有各种类型的抗体用于靶标蛋白,无论是单抗还是多抗,亦或是重组抗体,都 需要满足以下几点要求:
1. 识别目的蛋白的立体表位。这跟做Western Blot的抗体是有区别的,因为WB的抗体识 别的是蛋白的变性表位。
2. 识别甲醛交联后的立体表位。这跟做IP的抗体是有区别的。因为ChIP相对于IP需要甲 醛交联的过程,甲醛会在DNA和蛋白质,以及蛋白和蛋白的氨基/亚氨基之间形成共价键,所
以ChIP级的抗体还要识别甲醛交联后的目的蛋白。这跟免疫荧光的抗体有点类似。
3. ChIP级的抗体跟目的蛋白有足够强的相互作用,能够耐受高盐,低盐及多种去垢剂 (比如0.1% SDS,1%Triton X-100或NP-40)的清洗。
所以选择抗体时,最好选择文献报道可以用于ChIP实验的抗体,或抗体公司提供 ChIP-qPCR或ChIP-seq数据的抗体。若靶标蛋白无ChIP级抗体,且未见有ChIP文章的发表, 那么最好的办法就是寻找一种已经在交联实验中应用过的抗体(类似于ChIP实验的相关应 用)。具体而言,如免疫荧光(IF)和免疫组织化学(IHC)是在固定条件下进行的,因此在 这些分析中起作用的抗体很可能在ChIP实验中也可以使用。但值得强调的是,尽管抗体在IF 或IHC的固定条件下可识别蛋白质表位,但ChIP实验过程中的其他因素可能会阻止抗体发挥 良好作用。
ChIP过程使用的Buffer同样决定了IP的好坏
IP的另外一个关键因素是buffer,这包括binding buffer(超声用buffer)和wash buffer。
因为组蛋白与DNA的结合比较牢固,所以相对来说组蛋白修饰的ChIP更容易做,对 buffer的要求也不是太严格。但是对于很多转录因子来说,因为本身跟DNA不是特别紧密(很 多都是动态结合),在同一染色质区域,只有很少部分细胞可以捕获到目的蛋白和DNA的结 合,所以通过合适的buffer将目的蛋白结合的DNA与背景DNA区分并分离出来就显得很关键 了。
一般来说,选用的Buffer越剧烈,背景DNA去除的就会越干净,但同样的,目的DNA也 会被更多的清洗掉。反之,选用的buffer越温和,目的DNA得到的就会越多,但同样的,背景 DNA也就残留的越多。
对于去垢剂来说,离子型去垢剂(如SDS,SDC)比非离子型去垢剂剧烈得多。对于盐来 说,剧烈程度LiCl>NaCl>KCl。去垢剂的选择,盐和去垢剂的浓度都会对ChIP效果产生很大 影响。很多实验室或公司在这方面都有自己独到的buffer配方。
本文来自Active Motif
-
免疫荧光结果不理想,可能是固定剂和通透剂的锅!
“道理我们都懂,IF实验也做完了。可是,为什么我的蛋白定位和别人做的不一致呢?这数据我也不敢给老板汇报啊~555~”有小伙伴向小P哭诉。
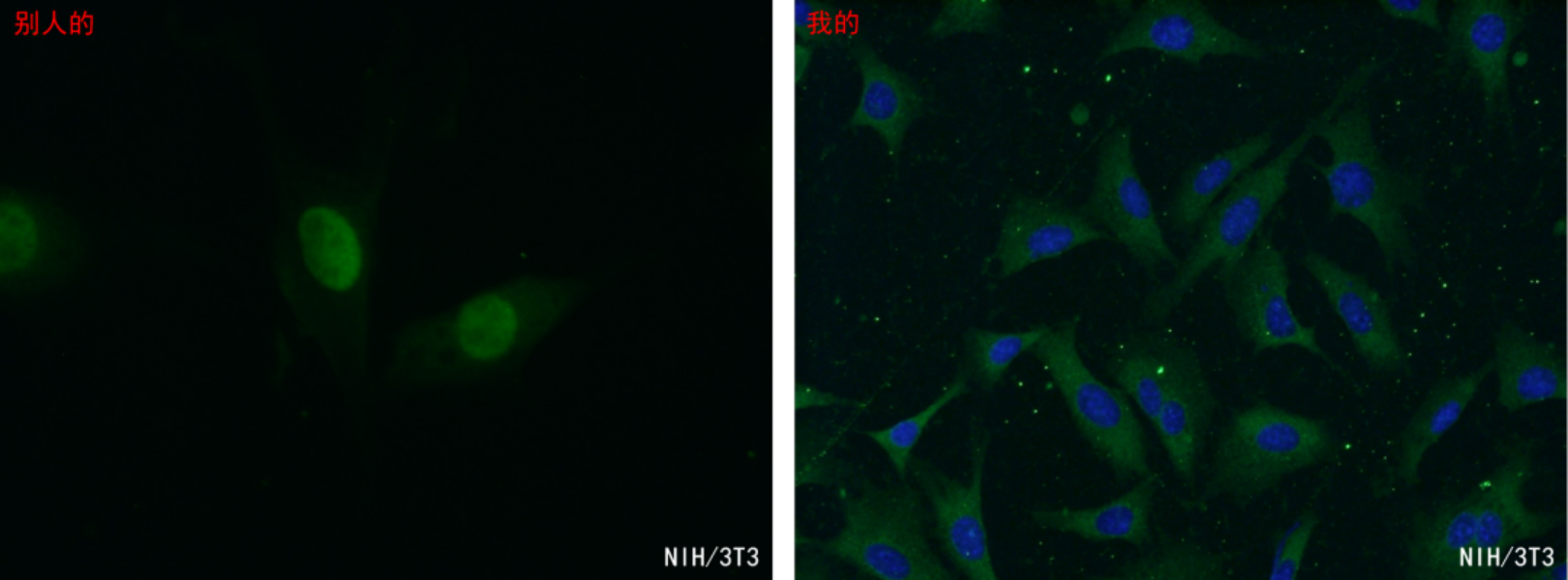
FEN1抗体(货号:14768-1-AP)染NIH/3T3细胞
FEN1是一种结构特异性核酸酶,理论上应在细胞核表达,前人研究中免疫荧光结果与预期一致,细胞核染色(左图)。
小伙伴使用相同的抗体anti-FEN1(货号:14768-1-AP)染乙醇固定的NIH/3T3细胞 ,结果细胞质着色,与预期及前人结果相悖(右图)。
小伙伴表示有亿点点委屈,为什么啊???
......
不要慌,作为抗体应用专家,免疫荧光小能手,小P这就给大伙儿梳理梳理,为什么会出现荧光信号不对的情况,究竟是谁的锅?
1. 固定剂的锅 做过细胞IF的同学都知道,在拿到样本之后,我们很重要的一步就是要对细胞进行固定。固定,顾名思义就是将细胞“固定”起来,这样能长久的保持细胞形态和抗原状态,让抗原能够与抗体更充分且更稳定地结合。
可有多少同学知道,固定剂也会影响蛋白(抗原)的亚细胞定位实验结果?
比如,我们研究部分核蛋白时发现如果采用乙醇固定,就会出现胞浆染色的结果。
B23/NPM1抗体(货号:60096-1-Ig)染MCF-7细胞
左图4%多聚甲醛固定MCF-7细胞(细胞核着色-阳性),右图乙醇固定(细胞质着色-非特异性着色)。
而当我们用E-cadherin抗体染细胞膜时,如果采用的是4%多聚甲醛固定,也会出现细胞核假阳性信号。
E-cadherin抗体(货号:20874-1-AP)为细胞膜着色
左图4%多聚甲醛固定MCF-7细胞(细胞核着色-非特异性着色),右图乙醇固定(细胞膜着色-阳性)。
显然,固定剂确实影响到蛋白(抗原)的亚细胞定位实验结果。不同固定剂的作用原理不同,不同靶蛋白及所用抗体特性不同,都可能影响到固定剂使用效果。因此选对合适的固定剂对一个准确可靠的IF结果是至关重要的。
上面与预期结果不一致的小伙伴其实就是因为采用了乙醇固定才导致了非特异性着色结果,前人的研究中均采用的4%多聚甲醛固定。
那么该如何挑选合适的固定剂呢?且往下看:
常用的固定剂种类很多,一般固定剂可分为两大类:可溶性溶剂和交联剂。可溶性溶剂比如丙酮、乙醇等能去除脂类物质并使细胞脱水,把蛋白质沉淀在细胞结构上。交联剂比如多聚甲醛可以通过自由氨基基团把生物分子桥连起来,形成一个相互连接的抗原网。
组织或细胞经过固定后可使胞内蛋白凝固,减少或终止外源性酶和内源性酶的反应;保持组织或细胞的抗原性,避免抗原发生弥散;保持组织和细胞的固有形态和结构。
不同类型固定剂优缺点如下:
根据多年抗体开发和蛋白检测经验,总结了一份【不同细胞器首选固定剂方法】,供大家参考:
当然,固定剂的选择其实是没有通用规则的,以上表格也是经验之谈,不排除有特殊情况。如果没有达到预期的实验效果,您也可以尝试更换其他固定试剂。
2. 通透剂的锅 说到固定剂,那就必须聊一下通透剂,通透剂没选好同样会造成IF结果不理想。
交联固定剂比有机溶剂能更完整的保持细胞结构,保存脂类物质,但也会因此而阻碍抗体-抗原的结合,甚至屏蔽抗原表位,造成阴性检测结果。因此可能需要增加一个通透步骤以使抗体能够顺利进入并接触抗原。我们可以根据靶标所处的位置进行选择使用或者不使用通透剂,以及选择何种强度的通透剂。
1)如果您检测的是胞外表位(细胞膜表面蛋白、膜整合蛋白的胞外段等),则无需进行通透,固定之后即可检测。
2)如果您检测的是胞内表位(膜整合蛋白的胞内段、细胞骨架蛋白、细胞器膜外蛋白等),需选择温和的细胞通透剂,比如Digitonin、Leucoperm、Saponin和Tween 20等,它能够在膜上打孔,增加细胞膜的通透性,使抗体进入胞质中,识别胞质中的表位。
3)如果您检测的是有膜细胞器内的表位(核内蛋白、线粒体内的蛋白等),则需要采用强通透剂,比如Triton X-100和NP-40等,它们可以部分溶解细胞核膜等细胞器膜结构,使抗体进入细胞器内部识别抗原并结合抗原表位。
3. 其他可能的锅 总而言之呢,免疫荧光结果不理想,可能的原因非常多,其中固定剂和通透剂的选择也至关重要的一步,希望大家要牢记!
除此之外的可能原因,小P这里根据多年的实验经验,总结了一份【免疫荧光疑难解析】,针对各种不理想情况分析了“锅”的归属,希望对大家有所帮助!
-
大分子WB很难?手把手教学来啦!
最近收到了不少客户关于大分子WB检测的咨询,由此可见大分子检测可谓是难倒一大批做WB的科研人员!
那么作为一家专业的抗体生产商,针对大分子抗体,500kD以上的超大分子,Proteintech又是如何检测的呢?
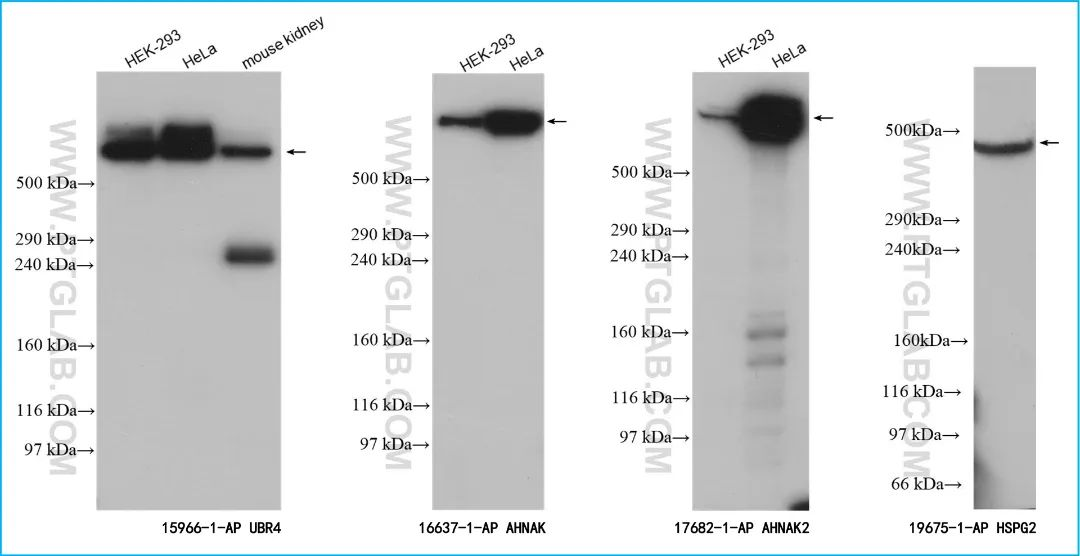
秉承着“助力科研”的理念和愿景,小P带着《Proteintech大分子WB疑难解析和检测方案》来啦~
大分子WB疑难解析做大分子WB检测,我们首先得弄明白:大分子WB的难点在哪里?只有弄清楚了难点在哪里,我们才能做出相应的对策。
那到底难在哪里呢?难点就在:大分子蛋白质的完整性容易被破坏。
那如何去保护大分子蛋白质的完整性不被破坏呢?我们可以从两个方面去改进:凝胶体系和蛋白样品制备。
(1)凝胶体系
我们目前使用的WB以Laemmli凝胶体系为主,Laemmli凝胶体系的优点我们就不必过多说明,关键是它的缺点大家是否了解?
(a)Laemmli凝胶的分离胶高pH值(8.8),易造成蛋白质碱性降解,如脱氨基作用等;(b)在Laemmli凝胶体系中含有半胱氨酸的蛋白质的氧化还原状态并不稳定;(c)Laemmli凝胶体系的制样过程中加入SDS sample buffer后,100℃煮样会造成ASP-Pro键断裂①。
由此可见Laemmli凝胶体系对大分子蛋白质完整性的保护是“极不友好”的,所以凝胶体系需要改变。
那到底哪种凝胶体系更加适合大分子WB检测呢?
其实早在十几年前,免疫学的科学家们就提出了Tris-Acetate凝胶体系用于大分子WB的检测,Tris-Acetate凝胶体系的中性pH值(7.0)完美的避开上述Laemmli凝胶体系的缺点,最大程度的保持大分子蛋白质的完整性。
为了验证Tris-Acetate凝胶体系的可靠性,严谨的Proteintech科研人员做了各种实验对比,结果如下图:
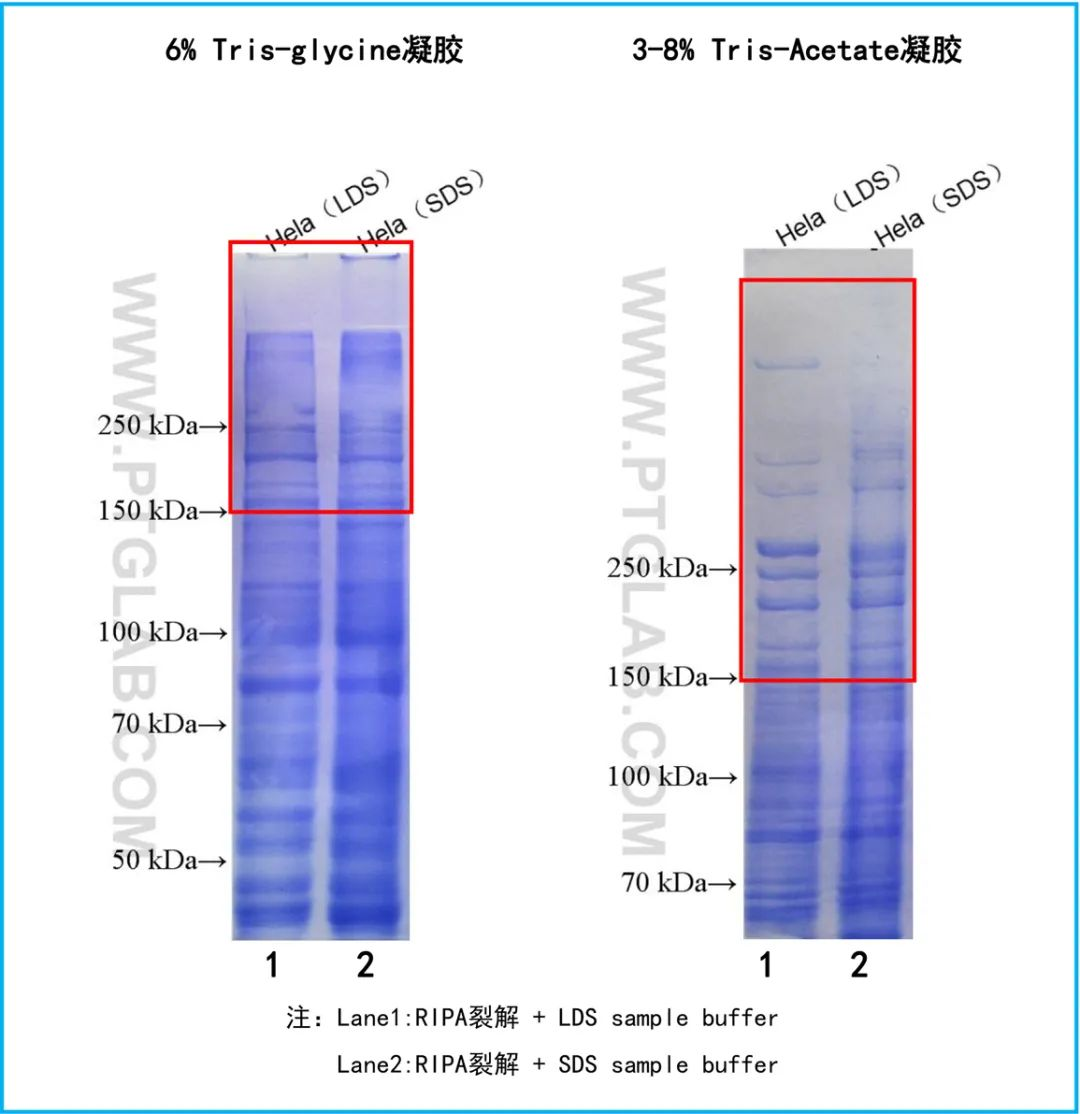
通过上述实验结果,可以很清晰地看到,Hela样品在Tris-glycine凝胶中150KDa以上的条带很少且模糊,尤其是250KDa以上基本看不到任何条带;而反观Tris-Acetate凝胶中150KDa以上的条带非常的清晰、锐利。
(2)蛋白样品制备
选择了合适的凝胶体系,接下来的关键步骤就在蛋白样品制备上了。裂解液的裂解强度对大分子蛋白质的完整性起到决定的作用,我们可以通过一张跑胶图片来分析:
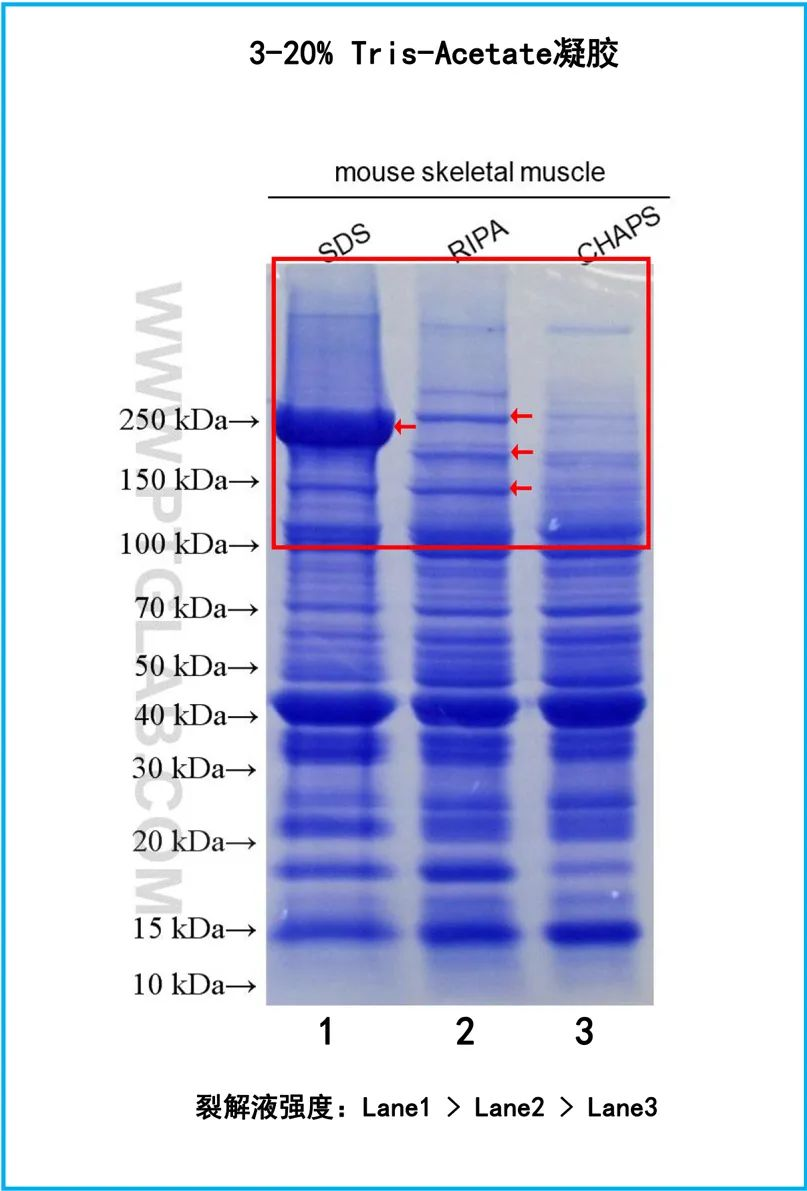
上图中是使用三种不同裂解强度的裂解液分别制备的mouse skeletal muscle的总蛋白样品,裂解液强度依次为Lane1(很强) >Lane2(中等)>Lane3(温和)。
我们仔细观察100KDa以上的蛋白条带可以发现在一定范围内裂解液的强度越温和时,100KDa以上的大分子蛋白条带会更多、更清晰。这是为什么呢?
可能存在的原因有:(1)当裂解液越强时,对蛋白质的溶解能力就越强,含量高的蛋白质溶解的就越多,后续对蛋白样品进行定量后,点样相同量的总蛋白时含量低的大分子蛋白质上样量就更低了;(2)当裂解液强时,大分子蛋白质容易被解聚,从而导致条带少。
为了避免大分子蛋白质的完整性在样品制备环节中被破坏,我们可以做以下三点改变:
(1)使用裂解能力温和的裂解液。如RIPA裂解液(中)、RIPA裂解液(弱)、Co-IP裂解液等,对于500KDa以上的大分子蛋白质检测甚至可以使用比上述裂解液更温和的CHAPS裂解液(配方见下文)。当然需要引起我们注意的是裂解液越温和溶解性越差,我们需要结合待测靶蛋白选用合适的裂解液。
(2)使用LDS-PAGE蛋白上样缓冲液。相比于的SDS,LDS不仅具有SDS相同的变性能力,还更加利于维持蛋白质的完整性。
(3)70℃水浴10分钟代替100℃煮样5分钟。70℃水浴可以有效的避免蛋白质ASP-Pro键断裂。
注:以上提供的只是大分子蛋白样品制备的最佳方案,并非常规SDS-PAGE蛋白上样缓冲液制样方式就一定不能用于大分子检测。
大分子WB检测方案一、样品制备
1. 根据下图配制CHAPS裂解液和LDS-PAGE蛋白上样缓冲液(4X)。
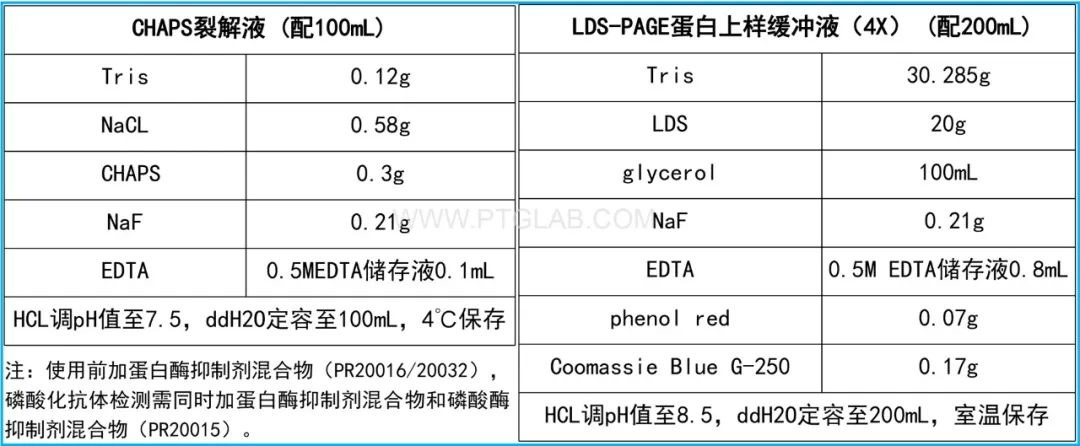
2. 细胞样品处理
a、瓶内裂解法(效果最佳):适用于所有的贴壁细胞
吸净培养基,用预冷的PBS清洗细胞表面2遍(动作轻柔,防止细胞脱落),尽可能吸取残留的PBS。在冰上按每1000万细胞加入1mL预冷的CHAPS裂解液于细胞瓶、培养板或培养皿中,用移液管吹散贴壁的细胞,对于贴壁紧的细胞也可使用细胞刮收集,收集裂解液,4℃冰箱或冰盒中摇晃30分钟,使其充分裂解。
b、离心法:适用于悬浮细胞和药物处理过的细胞
使用细胞刮收集细胞悬液(连同培养基一起收集),4℃,500 xg离心5分钟,收集沉淀,沉淀用预冷的PBS洗涤两遍,收集细胞沉淀,尽可能吸取残留的PBS。按每1000万细胞加入1mL预冷的CHAPS裂解液,4℃冰箱或冰盒中摇晃30分钟。
3. 动物组织样品:
取新鲜的动物组织,用预冷的PBS洗净组织块上附着的脂肪和血液等杂质,用滤纸吸干水分后称重。在离心管中将组织块剪碎,然后在冰上,按每100mg组织加1mL预冷的CHAPS裂解液。将样品转移到合适大小的预冷玻璃匀浆器中,在冰浴条件下对样品匀浆10-20次至充分裂解,收集匀浆液,4℃冰箱或冰盒中摇晃30分钟,使其充分裂解。
4. 4℃,15000xg离心15分钟,收集上清样品。
5. 使用BCA蛋白浓度检测试剂盒检测蛋白浓度,将样品分装成小份,同时每管按3:1加入LDS-PAGE蛋白上样缓冲液(4X),使样品中LDS-PAGE蛋白上样缓冲液的终浓度为1X,上下颠倒混匀,保存在-80℃冰箱。
6. 使用前室温解冻,每管补加新鲜的2M DTT溶液至终浓度为100mM,混匀,70℃水浴10分钟。
注:(1)不要对样品进行超声破碎;(2)解冻后的样品在2个小时内使用完;(3)样品不要反复冻融。
二、制梯度胶
(1)根据下图配制3M Gel buffer(15X)和40%Gel(37.5:1)。
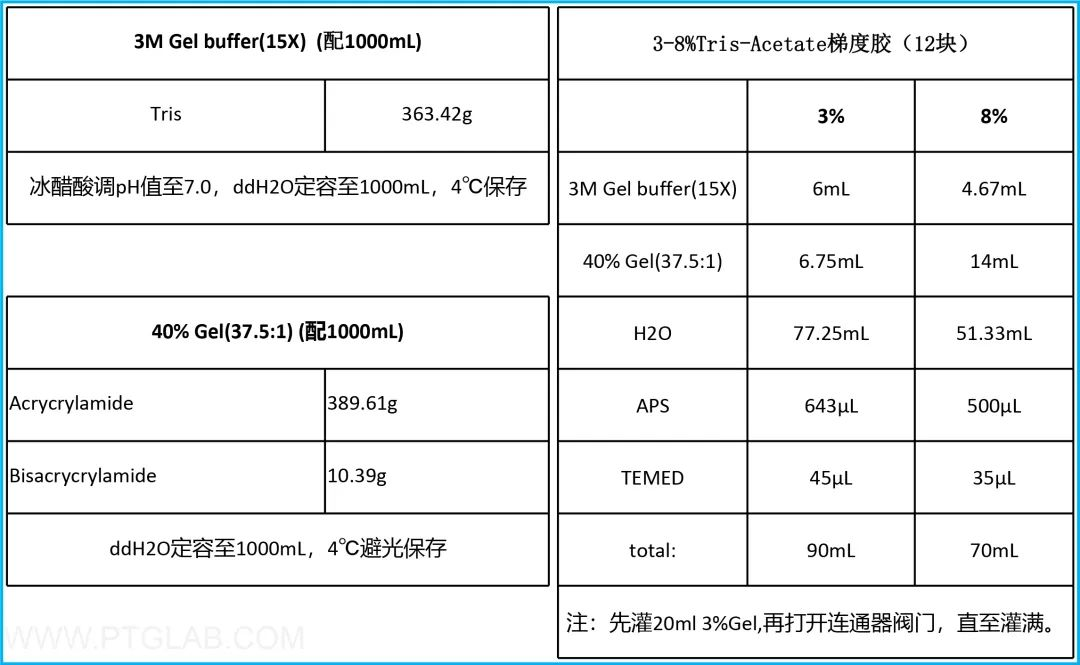
(2)按配方配制两种不同浓度的Tris-Acetate胶,使用梯度胶灌胶器先灌20mL 3%低浓度的Tris-Acetate胶,然后再将剩余的两种不同浓度的Tris-Acetate胶加入相应的梯度混匀仪杯体中,打开梯度混匀仪杯体的连通阀门开关进行梯度胶灌制,灌至小玻璃上边缘结束灌入,并插入梳子。
(3)室温水平静置2小时,直至醋酸胶完全凝固即可拔出梳子进行跑胶。
Tips:
(1)常用的Tris-glycine胶体系所用的胶母液C%值通常为3,而用于大分子检测的Tris-Acetate胶的胶母液C%值可以适当的降到2.6,这样可以让大分子的蛋白质完全进入凝胶中,避免堵塞在进样口。C%=Bisacrycrylamide/(Bisacrycrylamide+Acrycrylamide)*100%
(2)为让大分子蛋白完全进入凝胶,我们先灌制了2.5-3cm的3%的胶,然后再灌梯度胶。
(3)APS和TEMED应在浇注凝胶之前最后加入。APS溶液应新鲜制备,以确保凝胶具有良好的分辨率。
三、跑胶
1. 根据下图配制1X Running buffer。

2. 将梯度胶玻璃板上的残胶冲洗干净,放置在电泳槽中,加入1×Running buffer,将整个电泳槽放入冰水浴中,将标准品和蛋白样品加入胶的点样孔中,使用130v电压电泳,直至蓝色指示线跑出胶后结束电泳。
Tips:
3-8%的Tris-Acetate梯度胶在冰水浴中使用130v电压电泳通常90分钟指示剂可以完全跑出胶,此时凝胶最下面的Marker为50KDa左右,如需检测200KDa以上的目的带,可以在指示剂完全跑出胶后接着电泳30分钟(即总电泳时长2h),这样最下面的Marker为90KDa左右,200KDa以上的大分子蛋白质会拉的更开。
四、转膜
1. 根据下图配制1X Transfer buffer。
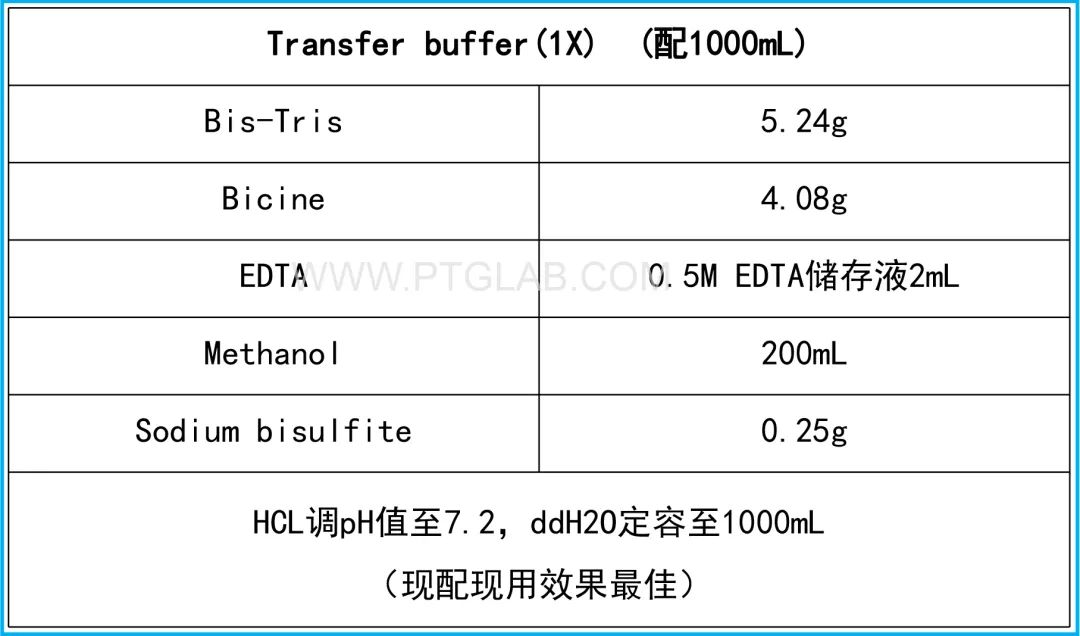
2. 将胶从电泳槽中取出,浸泡在转移缓冲液中,以海绵/滤纸/膜/胶/滤纸/海绵的方式,将其紧密排列,确保各个夹层之间没有气泡,采用20V恒压进行湿法转移过夜,保持整个转移仪在冰水浴中。
Tips:
转膜时不要将凝胶的上部分切掉,因为凝胶的上部分会有分子量较大的蛋白;强烈推荐过夜转移,过夜转移效率最佳。
五、免疫印迹
转移完成后,将膜取出,使用封闭液在37℃水平恒温摇床中封闭1小时,即可用于后续的免疫印迹实验,后续的免疫印迹实验与常规Laemmli凝胶体系步骤相同。
-
说明书太长?来看看这个吧!(PCR篇)
嘿,亲爱的朋友们!我们听到了你们的声音:说明书太长、太复杂了!明白了,谁不想快速搞定实验流程,然后去喝一杯咖啡呢?
所以,我们动手了!整理出一份“直击要害”的简易说明书,只有你最需要的部分。用我们的新版说明书,快速开始你的实验,省下时间享受生活吧!期待听到你们的使用心得哦!
PCR
-------
KOD One PCR Master Mix/Blue
-------


---------------
KOD Fx Neo
---------------


--------
KOD -Plus -Neo
---------


-
【qRT-PCR系列】 | 一针见血!让RNA病毒无处可藏!!
一步法qRT-PCR反应是指以RNA为起始模板,将RNA逆转录以及后续的靶标基因的扩增集于一管内完成,利用荧光信号对初始RNA模板进行定量或定性的技术。与逆转录和PCR扩增过程在两个管中完成的两步法qRT-PCR相比,一步法操作更为简便,降低了中间开盖导致的产物污染。并且,由于一步法qRT-PCR使用的是基因特异性引物,减弱了其他扩增产物的干扰,从而可获得更多的特异性目的cDNA。
东洋纺一步法qRT-PCR试剂盒THUNDERBIRD® Probe One-Step qRT-PCR Kit 【Code: QRZ-101】, 通过以高效率逆转录酶ReverTra Ace和高扩增性能的Tth DNA Polymerase两酶组合开发而来,主要应用于以TaqMan分析法的荧光定量PCR中。
在本产品中,两种酶与优化后的buffer组分组合,可以对微量RNA迅速定量;并且,可高灵敏度地检测出多种多样的RNA,不易受目的基因序列的影响;逆转录反应与PCR在同一反应体系中连续进行,反应液的分装操作一次就可以完成,适用于高通量分析,并降低了样品间交叉污染的危险性。
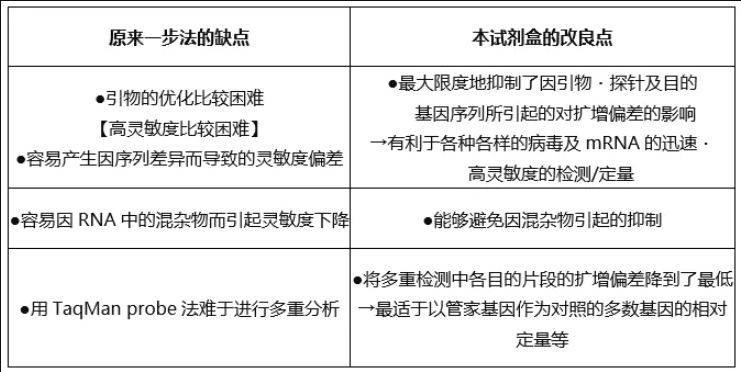
产品特征
迅速・高灵敏度
通过使用Probe的One-step qRT-PCR,可迅速高灵敏度地对微量RNA进行定量。
多重扩增低偏差
不易受目的基因序列的影响,可高灵敏度地检测出多种多样的RNA。
将多重检测(Multiplex)时各目的基因扩增的偏差降至最低。PCR抑制物抗性增强
可避免因血红素等的PCR抑制剂导致的灵敏度下降。
使用dUTP
通过添加Uracil-N-Glycosylase(UNG)*,能够防止因Carryover污染而导致的假阳性。
* 本产品中不含有UNG。
产品信息
【Code: QRZ-101】
THUNDERBIRD® Probe One-Step qRT-PCR Kit
(20μl*250 rxns)
文章来源东洋纺生物
-
大牛如何玩转巨噬细胞?近一年爆款文章回顾
1880年代,Ilya (Elie) Metchnikoff曾作为首个发现机体“内在治愈力”的科学家而闻名于世。起初这种能够吞噬碎片和微生物的移动细胞听起来太过危言耸听,被同期研究学者定义为“天方夜谭”。但这一理论最终被接受,并为Metchnikoff赢得了1908年的“诺贝尔生理学或医学奖”。这便是大名鼎鼎的巨噬细胞的前世今生。
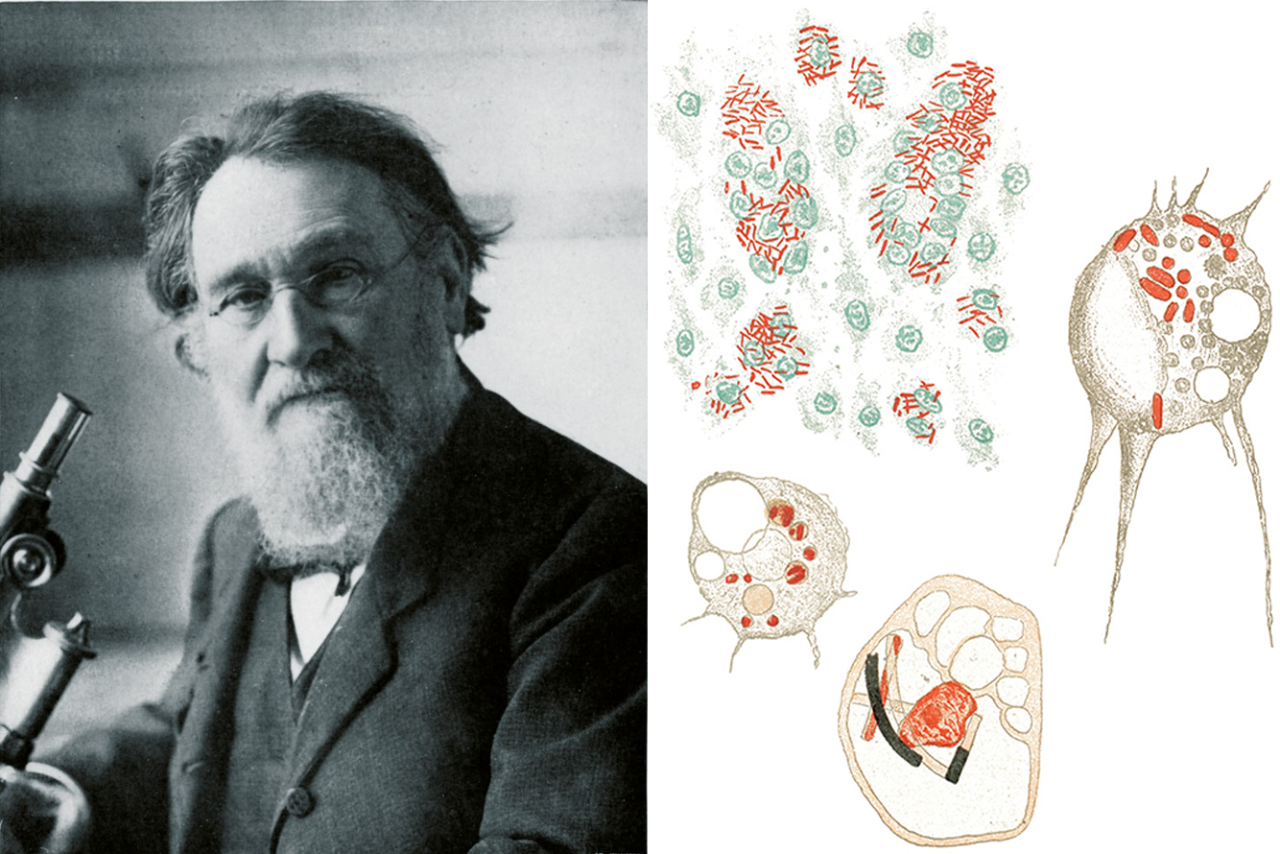
图1:Elie Metchnikoff和巨噬细胞(图片来自Immunity)
作为研究重点,大家对巨噬细胞来源、分布、分化、功能、与疾病的关系等早已有深入了解。长期以来,巨噬细胞被认为由骨髓中造血干细胞→普通髓系祖细胞→粒细胞/巨噬细胞祖细胞→单核细胞→巨噬细胞发育而来,广泛分布全身,在机体固有免疫中发挥重要作用。(点击本段文字查看更详细的巨噬细胞介绍)
既往研究可谓把巨噬细胞进行了360°的剖析。
这是否说明巨噬细胞的研究热潮将趋于平静?
恰恰相反。以macrophage为关键词在PubMed搜索,2014至2024年的十年间发文合计156356篇,年均发文14214篇。其中2021年达到发文量顶峰21261篇,2020增长率最快为16.07%。可见,大家对巨噬细胞的解析仍处于“打鸡血”的阶段。
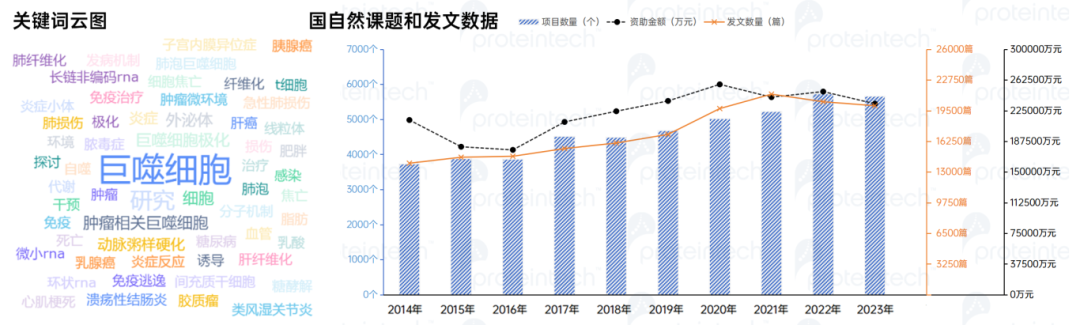
图2:巨噬细胞相关关键词、国自然课题和发文数据分析(数据来源国家自然科学基金委员会、citexs、NCBI和LetPub)
那么,大家最近都在围绕巨噬细胞进行什么研究呢?有哪些重磅突破?有哪些研究思路值得我们参考呢?
小P翻阅了过去一年中Proteintech助力的659篇巨噬细胞相关的SCI文章,筛选了6篇影响因子超30、具有重磅突破的文章。
下面,大家就和小P一起欣赏下这6个巨噬细胞相关的精彩故事吧~
巨噬细胞研究进展
1. 巨噬细胞与细胞衰老、肺癌
Clearance of senescent macrophages ameliorates tumorigenesis in KRAS-driven lung cancer
DOI:https://doi.org/10.1016/j.ccell.2023.05.004
英国伦敦大学学院儿童健康研究所Juan Pedro Martinez-Barbera和剑桥大学Daniel Muñoz-Espín研究团队合作在《Cancer Cell》(IF:50.3)杂志发表论文,证实:清除衰老巨噬细胞可改善KRAS驱动肺癌发生。
肿瘤微环境中衰老细胞的积累可通过衰老相关的分泌表型(SASP)以旁分泌的方式驱动肿瘤发生。利用全新的p16-FDR小鼠品系,该研究发现巨噬细胞和内皮细胞是小鼠KRAS驱动的肺肿瘤中的主要衰老细胞类型。通过单细胞转录组学,该研究确定了一组表达独特的促肿瘤SASP因子和表面蛋白的肿瘤相关巨噬细胞,它们也存在于正常衰老的肺中。在KRAS驱动的肺癌模型中,衰老细胞的遗传或衰老消融,或巨噬细胞耗竭,可导致肿瘤负荷的显著减少和生存率的增加。此外,该文献还发现人类肺癌前病变中具有衰老特征的巨噬细胞的存在,但不是在腺癌中。
本研究不仅解释了衰老巨噬细胞在肺癌发生和发展中的重要作用,展示了p16-FDR品系作为小鼠模型的强大应用能力,还突出了潜在的治疗途径和癌症预防策略。
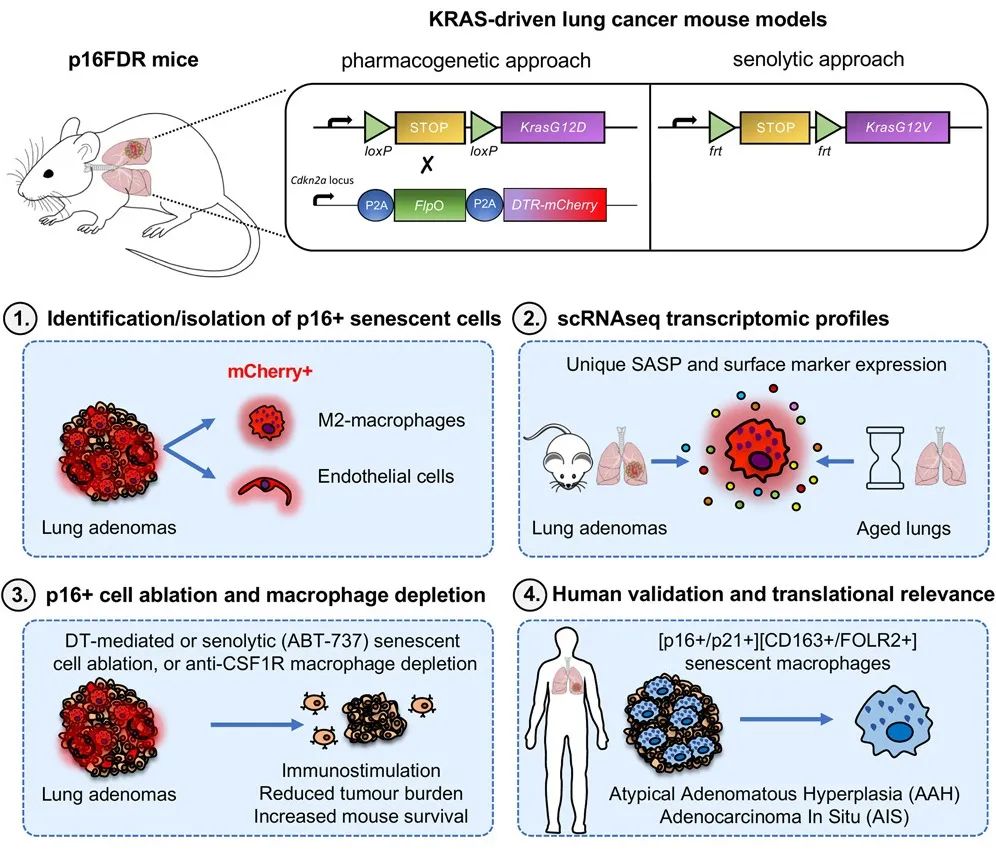
图3:KRAS驱动的肺癌示意图
Proteintech产品助力
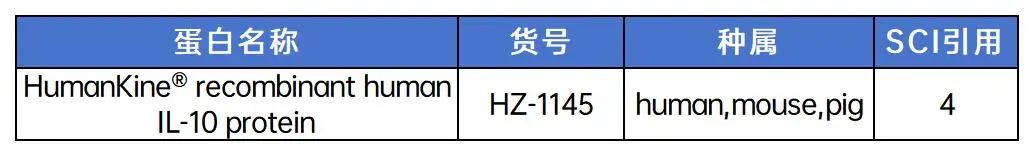
2. 巨噬细胞与肿瘤
YTHDF2 orchestrates tumor-associated macrophage reprogramming and controls antitumor immunity through CD8+ T cells
DOI:https://doi.org/10.1038/s41590-022-01398-6
美国希望之城国家医疗中心Michael A. Caligiuri 和Jianhua Yu研究团队在《Nature Immunology》(IF:30.5)杂志发表论文,发现:YTHDF2通过CD8+T细胞协调肿瘤相关巨噬细胞重编程并控制抗肿瘤免疫。
尽管肿瘤相关巨噬细胞(TAMs)在形成肿瘤微环境(TME)方面发挥着关键作用,但TAMs影响肿瘤微环境并促进癌症进展的机制仍不清楚。
该研究发现,N6-甲基腺苷阅读器YTHDF2能调节TAMs的抗肿瘤功能。TAMs中YTHDF2的缺乏可使TAMs重编程为抗肿瘤表型,并增强其抗原交叉呈递能力,从而抑制肿瘤生长,进而增强CD8+T细胞介导的抗肿瘤免疫。YTHDF2缺乏通过靶向干扰素-γ-STAT1信号传导促进TAMs重编程。YTHDF2在TAMs中的表达受白细胞介素-10-STAT3信号调节。利用Toll样受体9激动剂结合的siRNA选择性地靶向TAMs中的YTHDF2,可使TAMs重编程为抗肿瘤表型,抑制肿瘤生长并增强PD-L1抗体疗法的疗效。
总之,该研究结果描述了YTHDF2在协调TAMs中的作用,并表明抑制YTHDF2是加强癌症免疫疗法的有效方法。
Proteintech产品助力
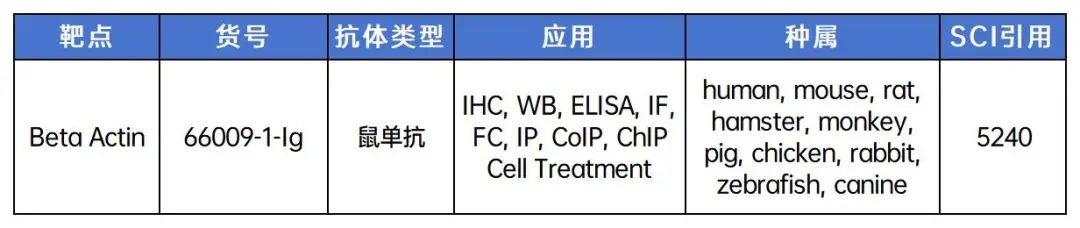
3. 巨噬细胞与脓毒症/驻留巨噬细胞
Soluble CD4 effectively prevents excessive TLR activation of resident macrophages in the onset of sepsis
DOI:https://doi.org/10.1038/s41392-023-01438-z
第二军医大学彭浩然教授、深圳市第三人民医院张政研究员和浙江大学医学院唐宏教授研究团队合作在《Signal Transduction And Targeted Therapy》(IF:39.3)杂志发表论文,证实:可溶性CD4可有效防止脓毒症发生时驻留巨噬细胞的TLR过度激活。
脓毒症早期因全身炎症而出现的T淋巴细胞减少通常与脓毒症感染的发病率和死亡率有关。研究团队此前证实,Toll样受体(TLR)介导的过度炎症需要足够数量的T细胞来抑制。然而,潜在的机制任然未知。
该研究揭示了CD4+T细胞与巨噬细胞的MHC II结合以下调TLR促炎信号传导。进一步研究发现,CD4+T细胞的CD4分子或胞外区域可溶性CD4(sCD4)与驻留巨噬细胞(resident macrophages)的MHC II直接接触,这对于防止LPS诱导和盲肠结扎穿刺(CLP)脓毒症模型中的TLR4过度激活是必要和充分的。sCD4血清浓度在LPS脓毒症发生后增加,表明其对过度炎症的代偿抑制作用。sCD4的参与使MHC II的胞浆结构域能够招募并激活STING和SHP2,从而抑制TLR4炎症所需的IRAK1/Erk和TRAF6/NF-κB激活。此外,CD4通过破坏促进MHC II内吞MHC II-TLR4结构域来颠覆TLR4的促炎质膜锚定。最后,sCD4/MHCII逆转信号特异性地干扰了TLR4而非 TNFR的高炎症反应,并且与巨噬细胞上CD4+细胞的CD40配体的抑制信号无关。
总的来说,足量的可溶性CD4蛋白可通过MHC II-TLR信号复合体的交替作用阻止巨噬细胞的过度炎症激活,这可能是有利于脓毒症预防治疗的新模式。
Proteintech产品助力
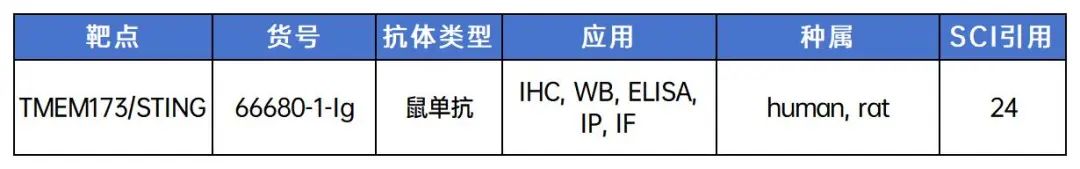
4. 巨噬细胞与自身免疫疾病(类风湿性关节炎)/巨噬细胞表型转化/代谢重编程
Metabolic reprogramming of proinflammatory macrophages by target delivered roburic acid effectively ameliorates rheumatoid arthritis symptoms
DOI:https://doi.org/10.1038/s41392-023-01499-0
四川大学张凌研究员团队在《Signal Transduction And Targeted Therapy》(IF:39.3)杂志发表论文,发现:通过靶向递送栎樱酸对促炎巨噬细胞进行代谢重编程,可有效改善类风湿性关节炎症状。
类风湿关节炎(RA)是一种常见的慢性炎症性疾病,通常累及关节。从抗类风湿关节炎草药大花秦艽(Gentiana macrophylla Pall.)中提取的栎樱酸(roburic acid,RBA)具有很强的抗炎活性。然而,由于其疏水性、缺乏靶向能力和功能机制不明确,其医疗应用受到了限制。
该研究构建了一种同时靶向CD44和叶酸受体的pH响应性双靶向RBA载药系统(RBA-NPs),并研究了其药理机制。在大鼠RA模型中,纳米载体能有效地将RBA递送至炎症部位,与游离RBA相比,治疗效果显著提高,并能有效降低炎症细胞因子水平,促进组织修复。后续分析表明,关节中的促炎型巨噬细胞(M1)被RBA重编程为抗炎型巨噬细胞(M2)。由于促炎和抗炎巨噬细胞的平衡在维持免疫平衡和防止RA过度炎症中发挥着重要作用,这种重编程可能是抗RA作用的原因。此外该研究还发现,RBA-NPs通过阻断 ERK/HIF-1α/GLUT1通路下调糖酵解水平,促使M1向M2表型转换。
总之,该研究不仅开发了一种靶向递送系统,显著提高了RBA的抗RA效率,还发现了一种潜在的分子靶点,可通过代谢重编程方式驱动巨噬细胞表型转化。
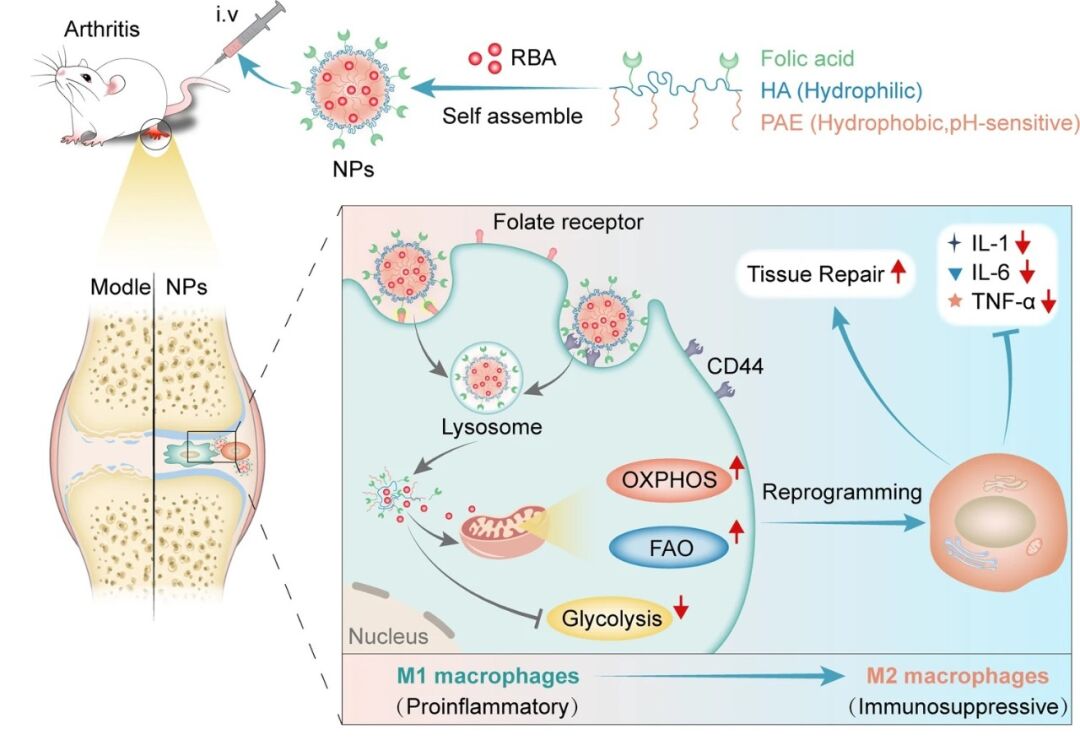
图4:RBA-NPs制备和RA治疗机制的示意图
Proteintech产品助力
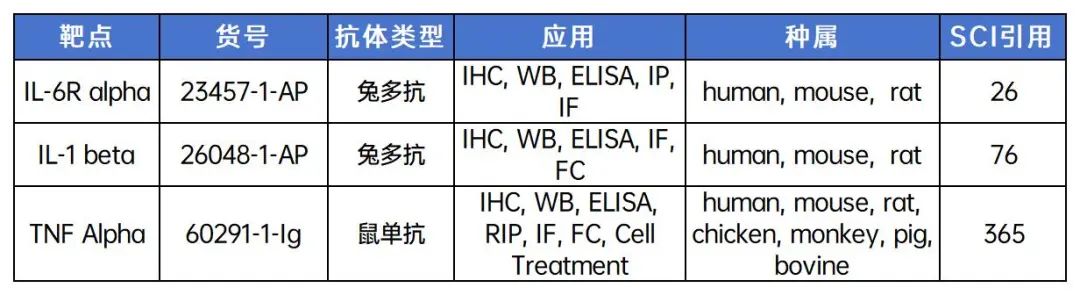
5. 巨噬细胞与肺炎
Expression of the readthrough transcript CiDRE in alveolar macrophages boosts SARS-CoV-2 susceptibility and promotes COVID-19 severity
DOI:https://doi.org/10.1016/j.immuni.2023.06.013
东京医科齿科大学Takashi Satoh研究团队在《Immunity》(IF:32.4)杂志发表论文,发现:在肺泡巨噬细胞中表达通读转录物CiDRE可提高SARS-CoV-2的易感性,并促进COVID-19严重程度。
SARS-CoV-2期间的肺部感染通过血管紧张素-I-转化酶2(ACE2)受体诱发细胞因子风暴。然而,COVID-19的确切机制尚不清楚。
该研究发现白细胞介素-10(IL-10)能诱导正常肺泡巨噬细胞中ACE2的表达,使它们成为SARS-CoV-2的载体。在仓鼠模型中抑制该系统可减轻SARS-CoV-2的致病性。全基因组关联和定量性状位点分析发现了一个IFNAR2-IL10RB通读转录本,即COVID-19感染性增强双受体(CiDRE)。该转录本在IFNAR2位点携带COVID-19风险变异的患者中高度表达。研究还表明,CiDRE通过肺泡巨噬细胞中的IL-10-ACE2轴发挥协同作用,并充当I型干扰素的诱饵受体。
总之,该研究表明,IL-10和CiDRE的高表达是造成严重COVID-19的潜在危险因素。因此,IL-10R和CiDRE抑制剂可能是有用的COVID-19疗法。
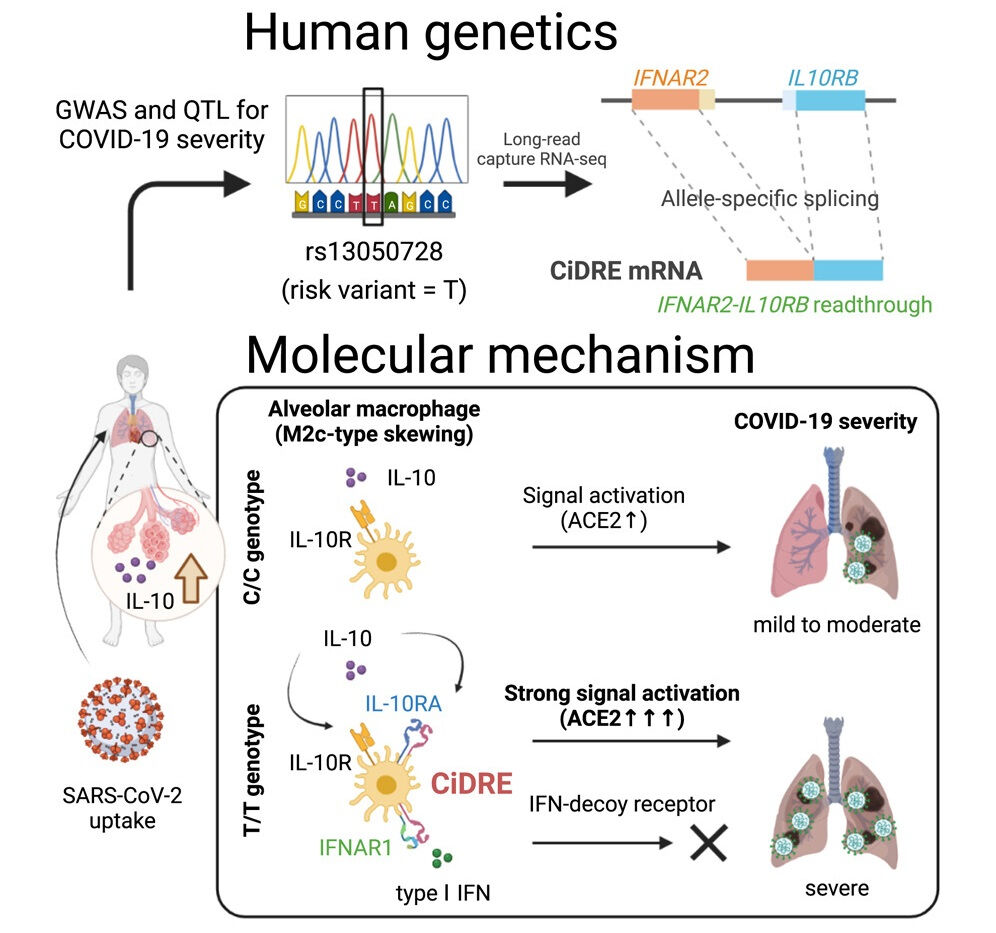
图5:IL-10和CiDRE影响COVID-19严重程度的机制
Proteintech产品助力
6. 巨噬细胞与疼痛、皮肤
Dermal macrophages set pain sensitivity by modulating the amount of tissue NGF through an SNX25-Nrf2 pathway
DOI:https://doi.org/10.1038/s41590-022-01418-5
日本奈良医科大学Akio Wanaka和Tatsuhide Tanaka研究团队在《Nature Immunology》(IF:30.5)杂志发表论文,发现:皮肤巨噬细胞通过SNX25-Nrf2途径调节组织NGF水平以调控疼痛敏感性。
外周神经细胞与免疫细胞之间的“交叉对话”在痛觉中非常重要。该研究在痛觉敏感性降低的转基因小鼠品系中发现分选蛋白25(sorting nexin 25,SNX25)是一种疼痛调节基因。在小鼠模型中,有条件地缺失单核细胞和巨噬细胞中的Snx25,而不是在外周感觉神经元中,降低了正常和神经病理性条件下的疼痛反应。使用Snx25cKO和野生型小鼠进行骨髓移植表明,巨噬细胞可调节痛觉敏感性。通过抑制泛素介导的Nrf2(一种激活Ngf转录的转录因子)降解,巨噬细胞中表达SNX25可增强神经营养因子NGF的表达。
因此,皮肤巨噬细胞通过向皮肤产生和分泌NGF来调控疼痛敏感性的阈值,它们可能与背根神经节巨噬细胞合作感知疼痛。
Proteintech产品助力
小结
不难看出,巨噬细胞作为具有高度可塑性和异质性的“多面手”,始终处于研究的核心地位。除了为人熟知的吞噬和免疫调节等功能外,巨噬细胞的更多“秘密”被研究人员们探索到:
(1) 巨噬细胞极化
巨噬细胞不同表型发挥不同功能(M1促炎、M2抗炎),其动态变化也决定着组织/器官在炎症和损伤中的命运。因此巨噬细胞极化与组织重构和再生、伤口愈合、血管生成、肿瘤(如上述文献2)、疾病(如上述文献4)等方面关联值得我们关注。
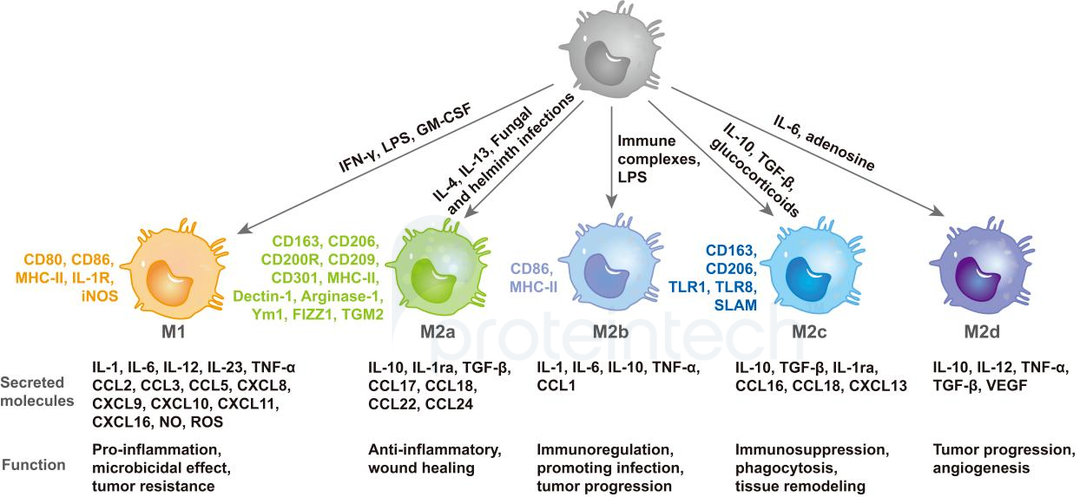
图6:巨噬细胞的极化,图源Proteintech
(2) 驻留巨噬细胞
驻留巨噬细胞概念也是近期研究扩展的。它们在人体中持续存在,和特化组织细胞具有稳定的空间和功能关联,如与脂肪相关的巨噬细胞与脂肪组织中的白色脂肪细胞共存[1]。
不同于造血干细胞和单核细胞来源的巨噬细胞,这种辅助细胞类型感知和整合局部和系统信息,为特殊的组织细胞提供生长因子、营养循环和废物清除。因此,我们可以关注其与组织生长、稳态和修复(如上述文献3)的关联性。
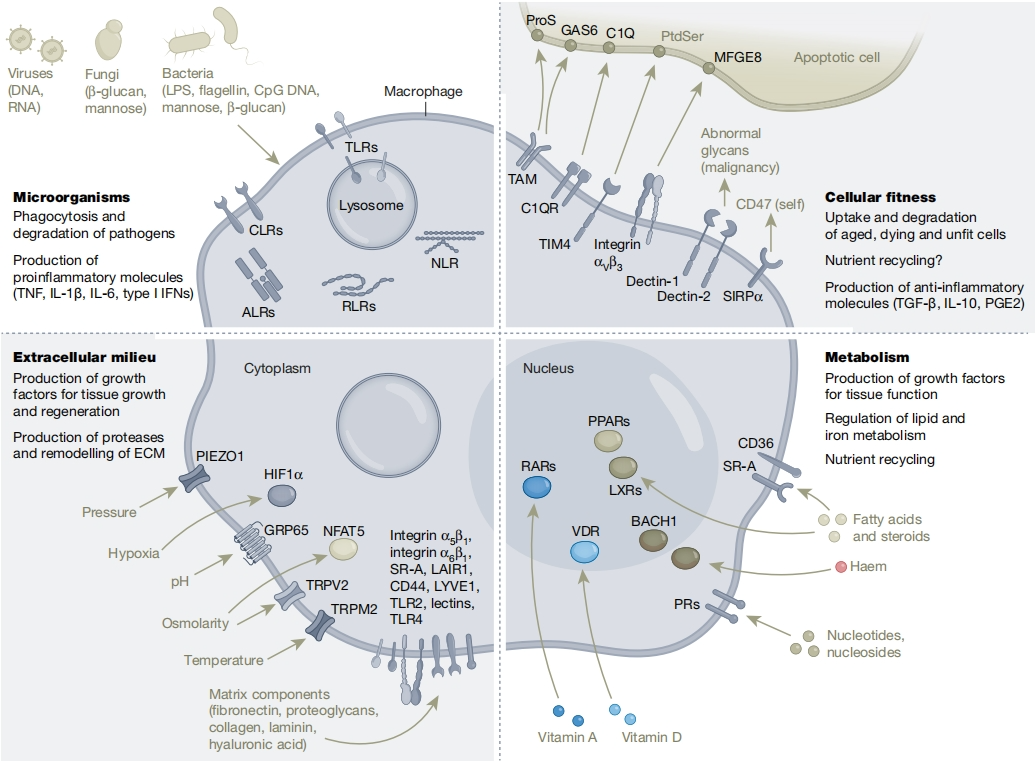
图7:组织驻留巨噬细胞的传感谱系和效应作用(图源参考文献1) (3) 代谢重编程
代谢重编程(如上述文献4)通过改变能量需求以应对不同的环境/压力胁迫,其中糖代谢重编程、脂代谢重编程、氨基酸代谢重编程等均与疾病发生和发展密切相关,其相关信号通路的关键蛋白也可能成为药物和治疗靶点。
(4) 肿瘤相关
被募集到肿瘤微环境中的巨噬细胞对肿瘤的发生、发展、侵袭、转移及血管生成等方面发挥重要作用(如上述文献1/2),因此如何调节肿瘤相关巨噬细胞(TAMs)成为重点。
(5) 其他疾病
除了肿瘤外,巨噬细胞在呼吸道清理、慢性炎症、自身免疫疾病、心脑血管疾病等方面的作用也是很好探索方向(如上述文献3/4/5)。
小P还列举了2023年国自然基金中标标题供大家参考。
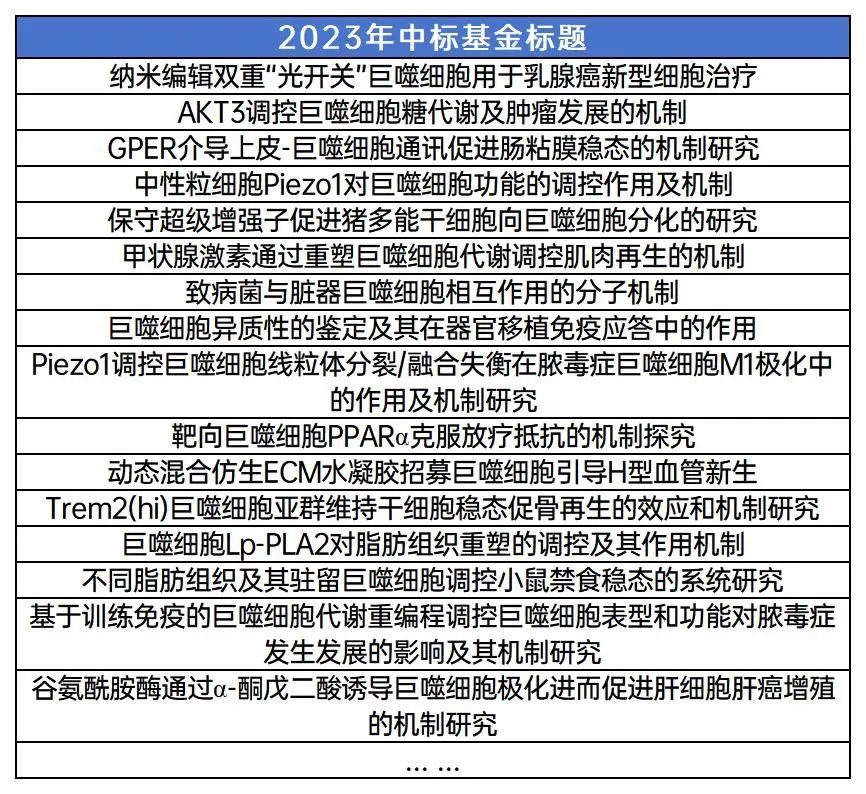
图8:线粒体相关中标基金标题(数据来源于国家自然科学基金委员会)
看完这些你有没有得到一些新的灵感和“解题思路”呢?如果文章对你有所启发,赶快和身边的小伙伴分享探讨一下吧!
除了上述列举的研究方向外,还有什么值得关注或者有趣的内容?也可以评论区讨论哦。
常用巨噬细胞标志物
为了方便大家查找,小P列举了一些常用的巨噬细胞标志物,可应用这些表型标记物来区分巨噬细胞和其他免疫细胞。小鼠巨噬细胞表达CD11b,F4/80,CSF-1R/CD115,人巨噬细胞表达CD68,CD11b,CD14,CD16,CD163,CD312,CSF-1R/CD115。
1. 常用M1和M2巨噬细胞标记物:
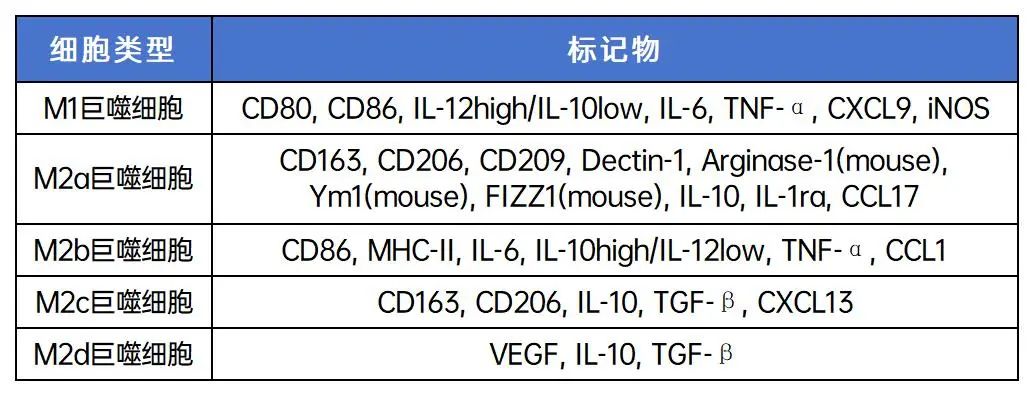
2. 不同组织中巨噬细胞及标记物:
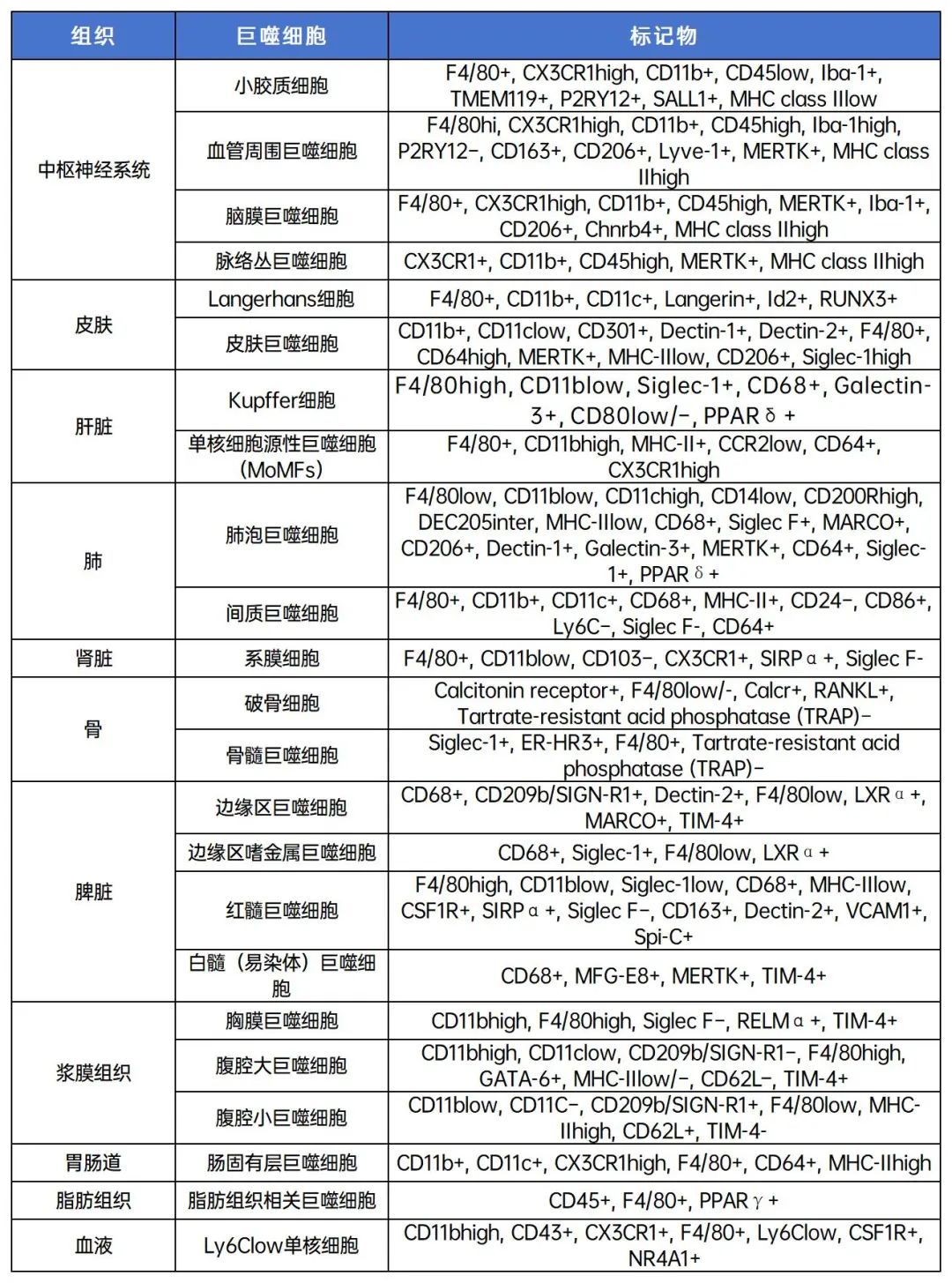
巨噬细胞标志物抗体推荐
针对以上大部分巨噬细胞标记物,Proteintech均已开发出了质量可靠的抗体产品,以帮助大家更好了解巨噬细胞。小P列举了一些抗体产品信息,希望对您的工作能有所帮助!
除抗体外,Proteintech还有更多巨噬细胞相关研究工具,如IHCeasy即用型免疫组化试剂盒、ELISA试剂盒、HumanKine®活性蛋白等,这里就不一一展示,有需要的老师可以直接添加文末客服咨询~
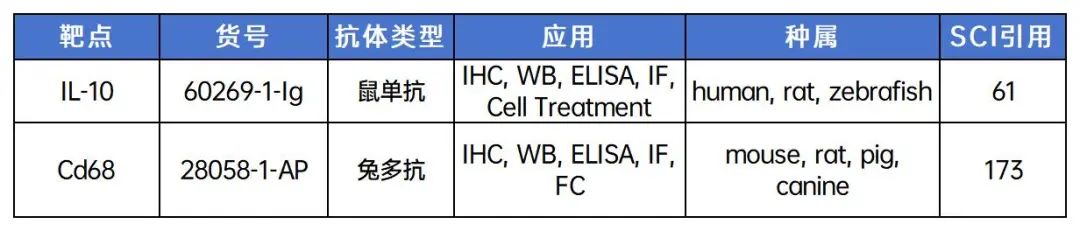
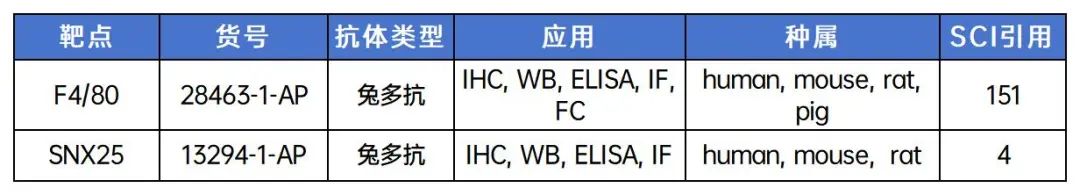
1. 巨噬细胞标记物常规抗体
(1) pan-macrophage marker
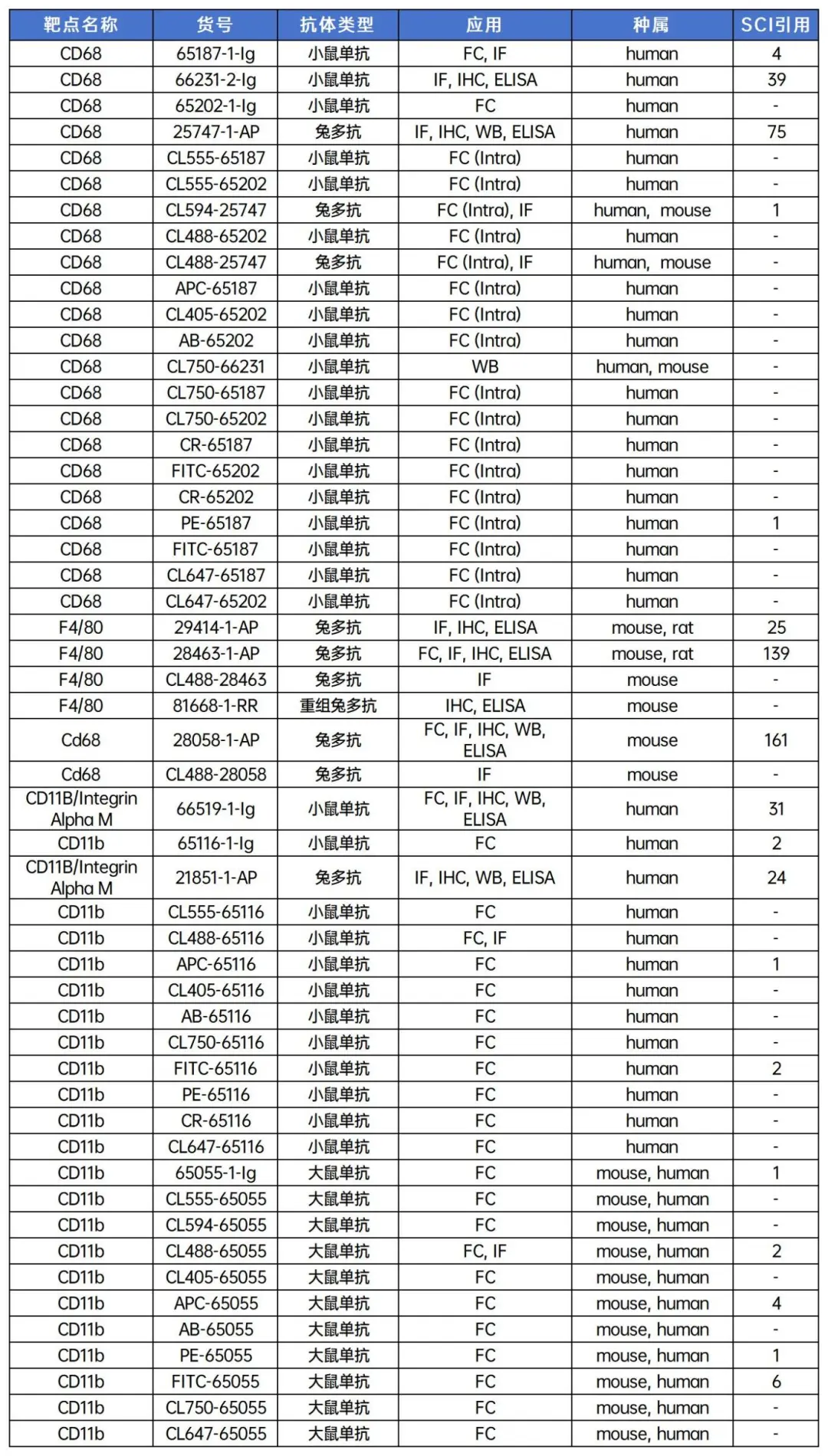
(2) M1 macrophage marker
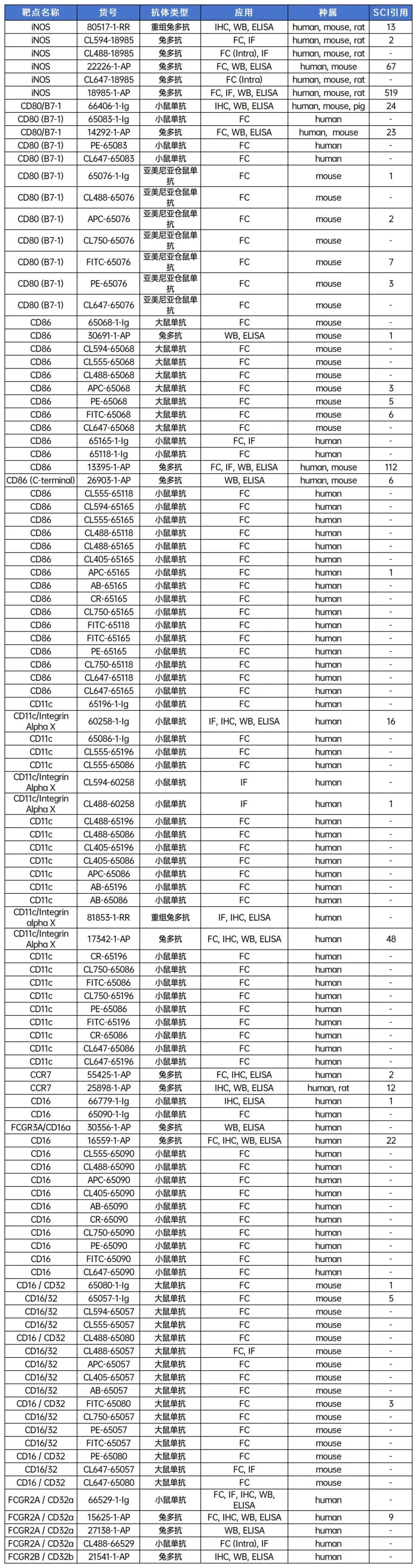
(3) M2 macrophage marker
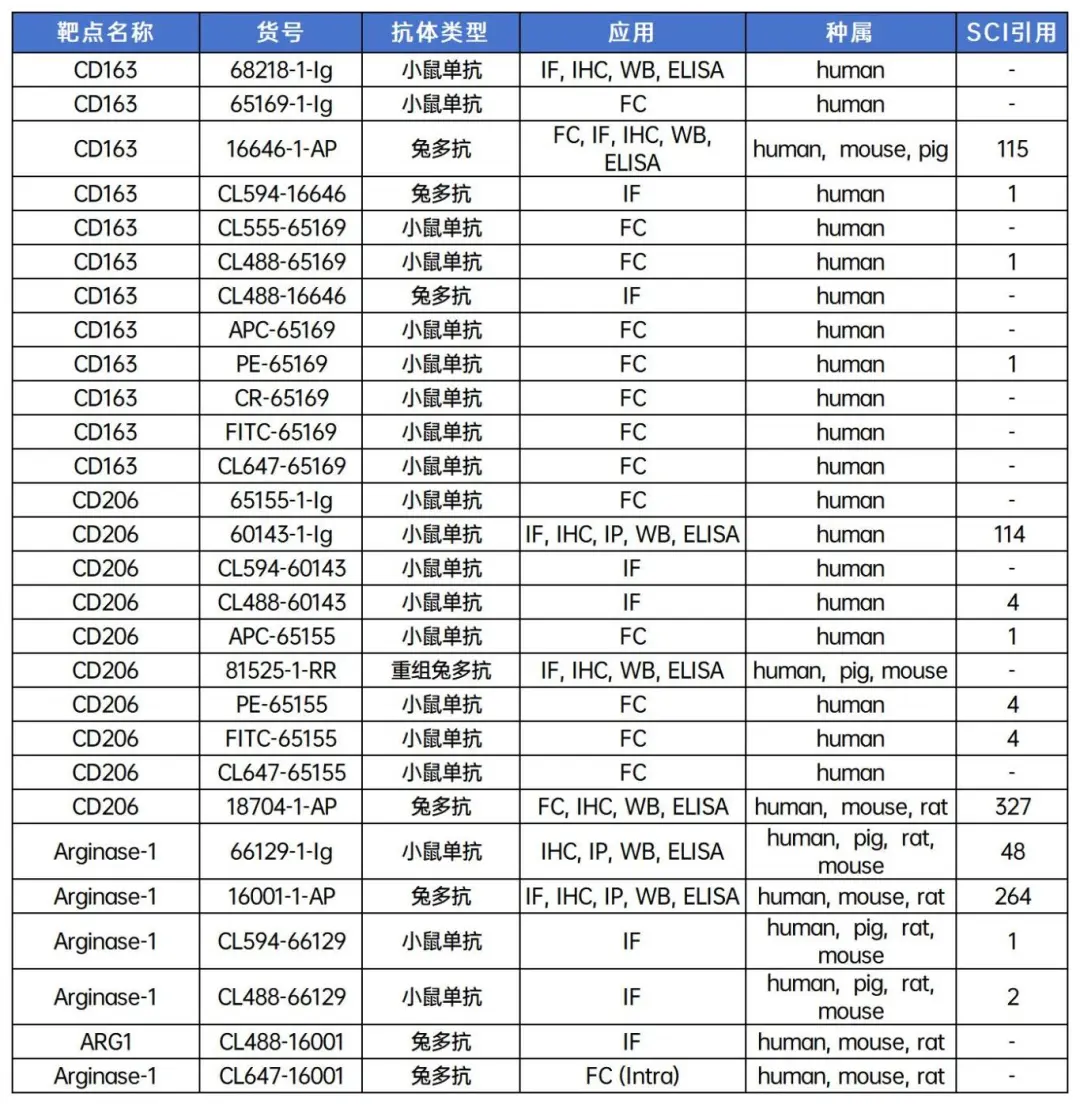
2. IHCeasy即用型免疫组化试剂盒
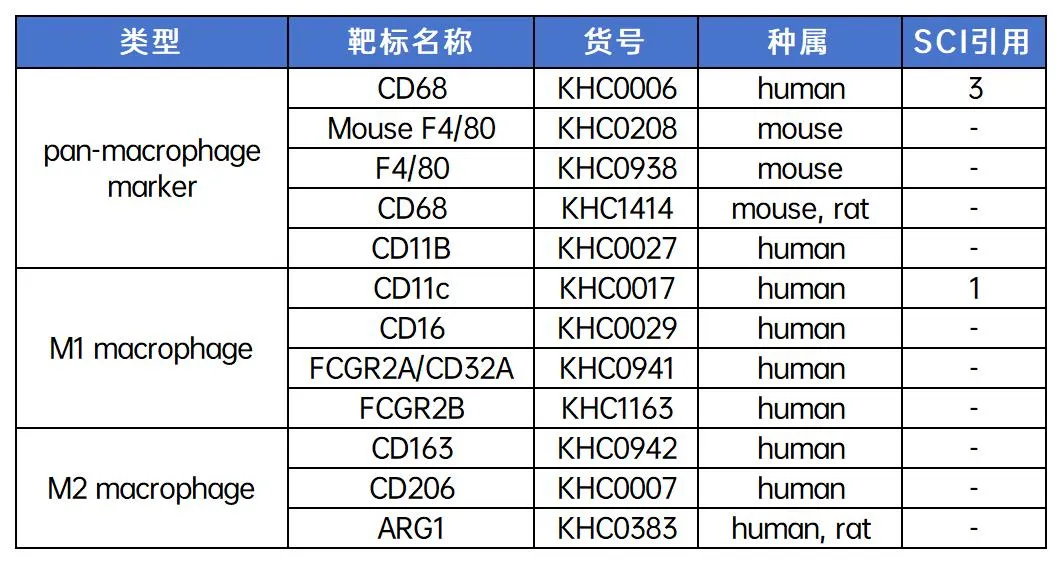
3. ELISA试剂盒
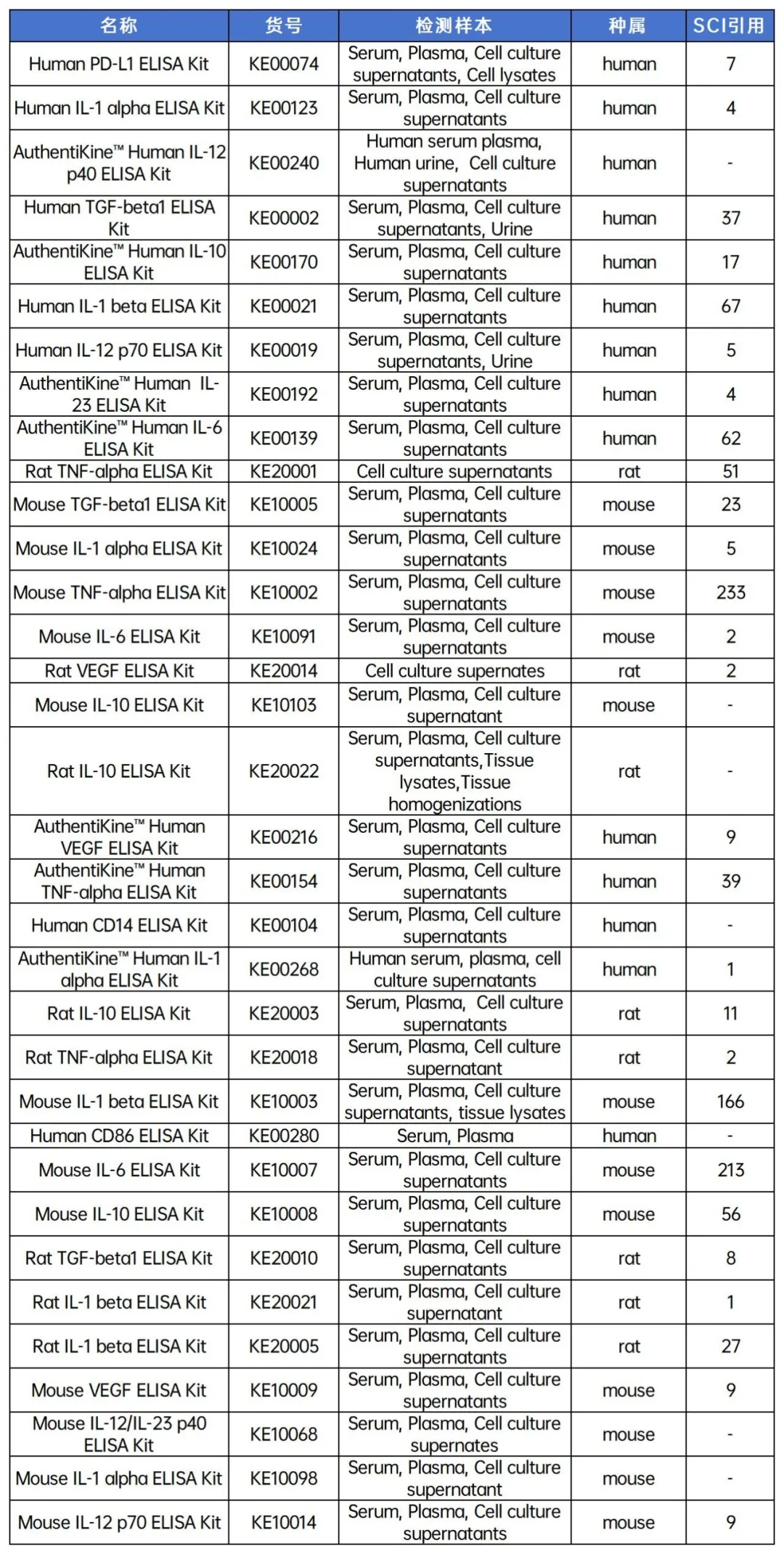
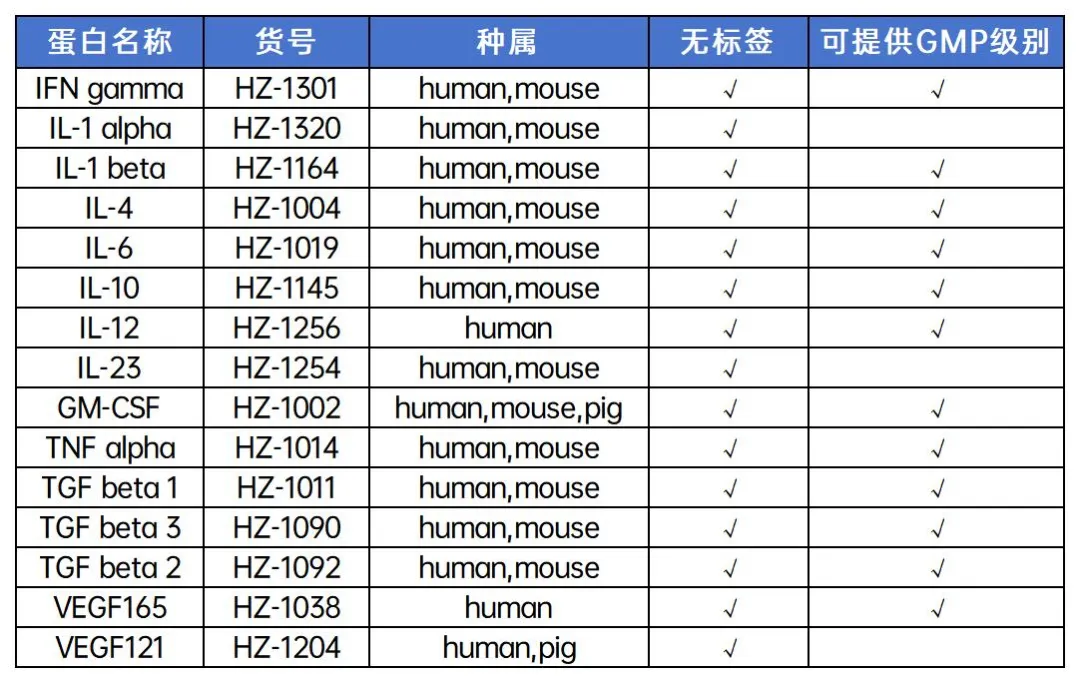
4. HumanKine®活性蛋白
参考文献
[1] Lazarov, T., Juarez-Carreño, S., Cox, N. et al. Physiology and diseases of tissue-resident macrophages. Nature 618, 698–707 (2023).
文章来源Proteintech